Интерес к препаратам висмута сильно возрос после открытия Helicobacter pylori: выяснилось, что лекарства на основе висмута в комбинации с антибиотиками способны эффективно подавлять жизнедеятельность бактерии, приводящей к развитию язвенных заболеваний. «Золотым стандартом» в эрадикации Helicobacter является висмута субцитрат.
Механизм действия соли висмута
Препараты висмута проявляют одновременно несколько эффектов:
- оказывает защитную функцию слизистой желудка благодаря способности образовывать защитную пленку и стимулировать выработку естественной слизи;
- уменьшает всасывание ряда антибиотиков, что позволяет использовать их для уничтожения Helicobacter;
- нарушает процессы синтеза в бактериальной клетке;
- уменьшает воспаление.
Показания к приему
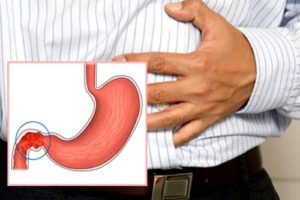
- язвенные поражения желудка и/или двенадцатиперстной кишки*;
- гастриты острые и хронические*;
- алкогольный гастрит;
- гастродуоденит*;
- обострение хронических воспалительных заболеваний органов ЖКТ.
* — в том числе, спровоцированные активностью Helicobacter pylori.
Список препаратов висмута
- «Де-Нол»;
- «Викаир»;
- «Викалин»;
- «Эскейп»;
- «Улькавис»;
- «Виканол Лайф»;
- «Витридинол».
«Де-Нол»
Производитель – Astellas Pharma Europe (Нидерланды).
 Выпускается в форме таблеток, содержащих 120 мг висмута субцитрата. Препарат практически не всасывается в кровь из ЖКТ. Может использоваться в терапии детей с 4-летнего возраста (под наблюдением врача).
Выпускается в форме таблеток, содержащих 120 мг висмута субцитрата. Препарат практически не всасывается в кровь из ЖКТ. Может использоваться в терапии детей с 4-летнего возраста (под наблюдением врача).
Для уничтожения Helicobacter рекомендуется применять средство в комбинации с прочими антибактериальными препаратами (метронидазол, амоксициллин, кларитромицин).
«Викаир»
Производитель – «Фармстандарт», «Валента», «Авексима» (Россия)
 Является комбинированным препаратом: помимо нитрата висмута (350 мг), содержит антациды (карбонат магния и гидрокарбонат натрия), порошок коры крушины (25 мг) и корневища аира (25 мг). Выпускается в таблетированной форме.
Является комбинированным препаратом: помимо нитрата висмута (350 мг), содержит антациды (карбонат магния и гидрокарбонат натрия), порошок коры крушины (25 мг) и корневища аира (25 мг). Выпускается в таблетированной форме.
Действие препарата направлено на взаимодействие основных компонентов: висмут проявляет защитные и антибактериальные свойства, антациды убирают симптомы повышенной кислотности желудочного сока, а растительные добавки оказывают слабительный и спазмолитический эффекты. Это позволяет нормализовать функции органов пищеварения.
«Викалин»
Производитель – «Обновление», «Авексима» и «Авва Рус» (Россия).
 Препарат похож по составу на «Викаир», но дополнительно содержит рутин (снижает проницаемость капилляров) и келлин «(как и аир, убирает спазмы гладких мышц органов ЖКТ).
Препарат похож по составу на «Викаир», но дополнительно содержит рутин (снижает проницаемость капилляров) и келлин «(как и аир, убирает спазмы гладких мышц органов ЖКТ).
Средство выпускается в виде таблеток.
«Эскейп»
Производитель – «Отисифарм» (Россия).
Является аналогом «Де-нола», содержит то же самое действующее вещество − висмута трикалия дицитрат в дозировке 120 мг. Выпускается в виде таблеток, покрытых плёночной оболочкой. Его цена, по сравнению с оригинальным препаратом, ниже на 200 руб.
«Улькавис»
 Производитель – КРКА (Словения).
Производитель – КРКА (Словения).
Лекарство также содержит субцитрат висмута (120 мг), поэтому его показания будут такими же и для прочих висмутсодержащих препаратов.
Выпускается в форме таблеток, покрытых оболочкой. Можно применять для лечения заболеваний ЖКТ у детей с 4-летнего возраста.
«Виканол Лайф»
Производитель – «ФармВИЛАР» (Россия).
В составе содержится 120 мг висмут трикалия дицитрата. Используется в качестве вспомогательного средства при лечении органов ЖКТ. Препарат не попадает в кровоток, т. к. не всасывается кишечником, выводится из него вместе с каловыми массами в неизменном виде.
«Витридинол»
Производитель – «ГИЛС и НП» (Россия).
Является очередным аналогом Де-нола с таким же составом. Выпускается в виде таблеток, покрытых плёночной оболочкой. В упаковке их 60. Показания у средства точно такие же, как и у других препаратов, содержащих висмут.
Особенности применения препаратов висмута
Общие рекомендации
- Висмутсодержащие средства необходимо принимать до еды (за 30 мин) и запивать небольшим количеством жидкости. Предпочтительно использовать только воду, и нежелательно запивать молоком, соками, чаем: эти напитки изменяют кислую среду в желудке, что уменьшает эффективность солей висмута.
- С этой же целью (см. выше) отказываются от приема антацидов до применения лекарства.
- Не рекомендуется комбинировать препараты висмута: это может привести к передозировке.
- Применять висмут с другими лекарственными средствами следует не одновременно, а с 2-3-часовыми промежутками, если не прописана другая схема.
Стандартный курс лечения гастрита и язвенной болезни – от 4 до 8 недель. Дозировка подбирается врачом индивидуально.
Уничтожение Helicobacter
Существует несколько схем, с помощью которых можно добиться положительных результатов:
- Первая линия (тройная терапия) – кларитромицин + ИПП + амоксициллин/метронидазол. Курс устанавливается индивидуально, обычно от 7 до 14 дней.
- Вторая линия – ИПП + висмута трикалия дицитрат + метронидазол + тетрациклин. Длительность курса определяет врач.
Эффективность лечения проверяют с помощью инструментальных анализов (на антигены Helicobacter и антитела к ней), ФЭГДС и/или биопсии.
Противопоказания
Препараты висмута противопоказаны в следующих случаях:
- период беременности и грудного вскармливания;
- почечная недостаточность;
- повышенная чувствительность к компонентам препаратов.
Для лечения детей висмутсодержащие препараты применяются только по показаниям и исключительно под наблюдением лечащего врача.
Есть ли побочные эффекты?
 окрашивание стула в черный оттенок;
окрашивание стула в черный оттенок;- потемнение языка;
- диспепсические расстройства: тошнота, рвота, запор или диарея;
- высыпания на коже, зуд;
- анафилактические проявления (отечность, крапивница);
- энцефалопатии (дистрофические изменения тканей головного мозга) при длительном применении или передозировке.
Альтернатива препаратам висмута
Несмотря на то, что соли висмута зарекомендовали себя в лечении расстройств ЖКТ, не все группы пациентов хорошо переносят эти средства.
Для замены используются фитопрепараты, а также синтетические препараты на основе сукральфата, омепразола, пирензепина. К этим лекарствам относятся:
- «
 Вентер»;
Вентер»; - «Гастроцепин»;
- «Омепразол»;
- «Домстал-О»;
- «Омез ДСР» и др.
Свойства указанных препаратов позволяют достичь эффектов, подобным тем, что оказывают соли висмута. Так, сукральфат образовывает защитное покрытие на слизистых и снижает активность пищеварительных ферментов; омепразол и пирензепин уменьшают продуцирование желудочного сока, а растительные средства в соединении с синтетическими препаратами усиливают регенеративные способности организма и мягко нормализуют работу органов пищеварения.


Препараты висмута
Общие сведения
В кислой среде желудка препараты висмута образуют на поверхности язв и эрозий защитную пленку, которая способствует рубцеванию язв и защищает слизистую от факторов агрессии. Кроме того, они увеличивают продукцию простагландинов и секрецию бикарбонатов, стимулируют выработку слизи и угнетают образование пепсина, а также обладают противомикробной активностью в отношении Helicobacter pylori местно в зоне язвы и в слизи, куда антибиотики проникают плохо.
Применяются висмута трикалия дицитрат (Вентрисол, Де-Нол, Трибамол), висмута субгаллат и висмута субнитрат (Бисмофальк), комбинированные препараты с висмутом (Викаир, Викалин).
Препараты висмута — противоязвенные средства. Оказывают гастропротективное действие. В кислой среде желудочно-кишечного тракта образуют на поверхности язв и эрозий защитную пленку, которая способствует их рубцеванию и предохраняет от воздействия желудочного сока.
Кроме того, препараты висмута оказывают бактерицидное действие на Helicobacter pylori — микроорганизм, который в ряде случаев способствует возникновению хронического гастрита и рецидивированию язвенной болезни.
Висмута субцитрат не всасывается из желудочно-кишечного тракта. Однако в течение всего периода лечения незначительное количество висмута может отщепляться от коллоида и поступать в кровь. Висмут, поступивший в кровь, экскретируется с мочой и его концентрация в плазме после окончания лечения быстро снижается. Выводится преимущественно с калом.
Язвенная болезнь желудка и двенадцатиперстной кишки; обострение гастродуоленита у больных язвенной болезнью; гастрит, ассоциированный с Helicobacter pylori.
Выраженное нарушение функции почек; беременность; лактация.
При приеме препаратов висмута наблюдается потемнение окраски кала, иногда это требует дифференциального диагноза с меленой. При длительном бесконтрольном приеме препаратов висмута возможны запоры или учащение стула, обратимое нарушение функции почек или почечная недостаточность, парестезии, бессонница, снижение памяти, энцефалопатия. Комбинированные ЛС, содержащие магний, оказывают послабляющее действие, содержащие алюминий – могут вызывать запоры, сухость во рту, тошноту, головную боль, головокружение, сонливость.
Препараты висмута способны окрашивать язык, губы и кал с темный цвет. При приеме висмута субнитрата возможно появление головной боли и метгемоглобинемии.
Не рекомендуется длительное применение больших доз висмута субцитрата (Де-Нол) из-за возможного развития обратимой энцефалопатии. Показано, что по окончании лечения концентрация активного вещества в плазме крови составляет около 5 мкг/л, а отрицательное действие наблюдается лишь при концентрации 100 мкг/л. Во время лечения препаратами висмута следует воздержаться от приема алкоголя.
За 30 мин до и после приема препаратов висмута необходимо воздержаться от приема напитков, твердой пищи, молока, антацидных препаратов.
При совместном применении препараты висмута уменьшают всасывание тетрациклина.
При одновременном применении препаратов висмута с другими средствами, содержащими висмут (викалин, викаир, ротер), повышается риск увеличения концентрации висмута в крови.
Соединения висмута нашли широкое применение в современной гастроэнтерологии, а наиболее часто используемым препаратом среди них является висмута трикалия дицитрат. Он обеспечивает защиту слизистой от воздействия различных повреждающих факторов и позволяет
Bismuth-based drugs are widely used in modern gastroenterology. Among them the most commonly used is bismuth subcitrate potassium. It protects the mucosa from the effects of various damaging factors, and anti-Helicobacter activity allows to overcome resistance of H. pylori to antibiotics, increasing the efficiency of pharmacotherapy.
Висмут (Bi) — относительно редкий элемент, обладающий не только металлическими свойствами, но и характеристиками, близкими к полупроводникам и изоляторам, поэтому иногда классифицируется как полуметалл или металлоид.
Bi (III) легко гидролизуется в водных растворах и имеет высокое сродство к кислороду, азоту и серосодержащими лигандам, Bi (V) является мощным окислителем в водном растворе и неустойчив в биологических системах [1].
Препараты висмута
Соединения висмута вошли в медицинскую практику со времен средневековья, а первый научный доклад о содержащем висмут препарате для лечения диспепсии был сделан в 1786 г. [1]. На сегодняшний день самое широкое применение соединения висмута нашли в гастроэнтерологии, а наиболее часто используемыми среди них являются висмута субсалицилат и коллоидный субцитрат (висмута трикалия дицитрат, ВТД) [2, 3] (табл. 1).
_575.gif)
Висмута субсалицилат во многих странах используется в качестве безрецептурного препарата для быстрого купирования изжоги, тошноты и диареи.
Коллоидный висмута субцитрат нашел применение в первую очередь для лечения заболеваний, ассоциированных с хеликобактерной инфекцией, а также как пленкообразующий гастропротектор. Именно этот препарат представляет наибольший интерес с точки зрения фармакологических свойств и клинического применения.
Перспективным представляется применение радионуклидов висмута (например, 213 Bi) для диагностики и лечения различных опухолей — лимфом, лейкемии [4, 5].
Висмута трикалия дицитрат
Взаимодействие со слизистой
На поверхности слизистой ВТД образует гликопротеин-висмутовые комплексы, по сути представляющие собой диффузионный барьер для HCl, который усиливается за счет дополнительного повышения вязкости пристеночной слизи [6, 7]. Этот процесс является рН-зависимым и ослабевает по мере повышения рН [8]. Если при нейтральном рН ВТД преимущественно находится в коллоидном состоянии, формируя структуры [Bi6O4(cit)4] 6- и [Bi12O8(cit)8] 12- , то при рН 2+ -чувствительный рецептор (CaSR), активируемый в норме внеклеточным Са 2+ и обеспечивающий повышение внутриклеточного Са 2+ , MAP-киназной активности и, в итоге, пролиферацию эпителиальных клеток слизистой желудка [22].
В экспериментальных исследованиях на слизистой толстой кишки мышей показана способность ионов Bi (III) за счет антагонизма с ионами Fe (III) подавлять активность неамидированного гастрина и, таким образом, возможность снижения избыточной гастрин-обусловленной пролиферации клеток [23].
Антихеликобактерная активность
Бактерицидное действие ВТД имеет очень важное значение. Под действием ионов висмута H. pylori теряет способность к адгезии, снижается подвижность микроорганизма, происходит вакуолизация и фрагментация клеточной стенки, подавление ферментных системы бактерий, т. е. достигается бактерицидный эффект (в отношении как вегетативных, так и кокковых форм H. pylori) [24–26]. Этот эффект при монотерапии ВТД хотя и незначителен (находится в пределах 14–40%), но не подвержен развитию резистентности и резко потенцируется при одновременном назначении с антибиотиками.
Висмут проникает в H. pylori, преимущественно локализуясь в области клеточной стенки микроорганизма. Он активно взаимодействует с нуклеотидами и аминокислотами, пептидами и белками H. pylori. Хотя молекулярные механизмы антихеликобактерного действия соединений висмута изучены не полностью, ясно, что основными мишенями в микроорганизме все же являются белковые молекулы (в том числе ферменты). Экспрессия примерно восьми белков подвергается up- или down-регуляции при действии ионов висмута [27, 28].
J. R. Lambert и Р. Midolo сформулировали основные молекулярные механизмы антихеликобактерного действия препаратов висмута [29], впоследствии дополненные другими исследователями [27]:
1) блокада адгезии H. pylori к поверхности эпителиальных клеток;
2) подавление различных ферментов, продуцируемых H. pylori (уреаза, каталаза, липаза/фосфолипаза, алкилгидропероксидредуктаза и др.), и трансляционного фактора (Ef-Tu);
3) прямое взаимодействие с белками теплового шока (HspA, HspB), нейтрофил-активирующим белком (NapA), нарушение структуры и функции других белков;
4) нарушение синтеза АТФ и других макроэргов;
5) нарушение синтеза, структуры и функции клеточной стенки и функции мембраны;
6) индукция свободнорадикальных процессов.
Одним из механизмов антибактериального действия ионов висмута является их взаимодействие с комплексом клеточной стенки/гликокаликса, имеющимся у некоторых микроорганизмов (в том числе у H. pylori), с вытеснением двухвалентных катионов Mg 2+ и Ca 2+ , необходимых для построения полисахаридных цепочек. При этом происходит локальное ослабление участков гликокаликса и выпирание клеточной стенки/мембраны через образовавшиеся «окна», что приводит к нарушению функционирования микроорганизма и может активировать аутолитические процессы, приводящие к его гибели [30].
Предполагается, что попадание висмута в H. pylori опосредуется через железотранспортные пути, а проникнув, он взаимодействует с участками связывания Zn (II), Ni (II) и Fe (III) белков и ферментов, нарушая их функцию [31, 32]. Например, связывание ионов висмута с малыми цитоплазматическими белками Hpn и Hpnl приводит к резкому нарушению их детоксицирующей и аккумулирующей функции «хранилища» для ионов Ni [33].
H. pylori характеризуется необычной версией шаперонина GroES (т. е. HpGroES), который обладает уникальным C-концом, богатым гистидином, цистеином и имеющим три металл-связывающих остатка (с Zn (II)), что обеспечивает сворачивание полипептидных цепей с формированием четвертичной структуры белка. Висмут-содержащие препараты прочно прикрепляются на этом сайте, вытесняя связанный цинк и, следовательно, вызывая резкое нарушение функции шаперонина HpGroES [34].
Препараты висмута, проникая в H. pylori, способны индуцировать мощный окислительный стресс в микроорганизме, что приводит к торможению деятельности многих ферментов в целом. Потенцируется прооксидантное действие подавлением активности тиоредоксина и алкилгидропероксидредуктазы (TsaA) микроорганизма [27, 28].
Ингибирование таких важных для микроорганизма ферментов, как протеаза и уреаза, является доказанным фактом в развитии антихеликобактерного эффекта ВТД [4]. В минимальной ингибирующей концентрации ВТД подавляет общую протеазную активность микроорганизма примерно на 87% [28].
Большое внимание привлекает взаимодействие висмута с ферментами цикла трикарбоновых кислот микроорганизма (фумаратредуктазы, фумаразы), обеспечивающего образование ряда биохимических прекурсоров (α-кетоглутарат, сукцинил-КоА, оксалоацетат) и работающего как источник образования АТФ. В результате уменьшается продукция макроэргов и подавляются многие энергозависимые процессы (в том числе репаративные, двигательные), что отражается, например, на скорости колонизации микроорганизмом различных отделов желудка [35, 36]. Потенцируется этот эффект блокадой локализованного в микробной стенке/мембране дитиольного фермента Na + /K + -АТФазы, с которым ионы Bi образуют стабильный комплекс [24].
В качестве еще одной ферментной мишени препаратов висмута рассматривается алкогольдегидрогеназа, участвующая в продукции ацетальдегида, который, секретируясь микроорганизмом, оказывает подавляющее действие на локальные защитные факторы слизистой, ингибируя секрецию белка и нарушая связывание пиридоксальфосфата с зависимыми ферментами [37].
Важное значение имеет также подавление висмутом активности фосфолипаз С и А2 H. pylori [38, 39]. В качестве новых мишеней для антихеликобактерного действия ВТД обсуждаются S-аденозилметионинсинтаза, альдолаза, фруктозобисфосфат и протеин S6 30S-субъединицы рибосомы [39].
Фармакокинетика ВТД
После перорального приема ВТД концентрация висмута в слизи желудка и слизистой сохраняется в пределах трех часов, после чего резко падает вследствие нормального обновления слизи [40]. Несмотря на то, что небольшая часть микропреципитатов ВТД может проникать в микроворсинки и путем эндоцитоза попадать в клетки эпителия, точные механизмы транспорта висмута в системный кровоток до настоящего времени неизвестны. Однако очевидно, что этот процесс происходит преимущественно в верхнем отделе тонкой кишки [41].
Биодоступность препаратов висмута низкая и у ВТД составляет 0,2–0,5% от введенной дозы [42, 43]. Н2-гистаминоблокаторы и ингибиторы протонной помпы могут увеличивать этот показатель [44]. После попадания в кровь препарат больше чем на 90% связывается с белками плазмы.
Измерение концентрации висмута в крови и моче после курсового применения ВТД в дозе 360 мг/сут в течение 4–6 недель показало большую вариабельность этого показателя. Так, концентрация висмута в крови варьировала от 9,3 до 17,7 мкг/л и выходила на плато примерно к 4-й неделе применения препарата [45]. В отдельных исследованиях были зафиксированы более высокие уровни препарата в крови (33–51 мкг/л), однако это не сопровождалось развитием побочных эффектов [46, 47]. Концентрация висмута в крови, как и площадь под фармакокинетической кривой, выше в том случае, если препарат принимается утром, по сравнению с ранним вечерним приемом [48].
В исследованиях на животных показано, что преимущественное накопление препарата происходит в почках и в значительно меньшей концентрации он обнаруживается в легких, печени, мозге, сердце и скелетной мускулатуре [49].
Особенности метаболизма и элиминации висмута изучены недостаточно. Период полувыведения висмута из крови и мочи у пациентов с интоксикацией составляет соответственно 5,2 и 4,5 дня [50]. У здоровых добровольцев и пациентов с гастритом клиренс составляет примерно 22–102 мл/мин (медиана 55 мл/мин) и Т1/2 около 5 дней (Т1/2 β до 21 дня), что свидетельствует о тканевом депонировании препарата и его медленной мобилизации оттуда [51]. На выведение препарата оказывает влияние функция почек, и при ее ухудшении почечный клиренс препарата может снижаться. Некоторые фармакокинетические показатели ВТД приведены в табл. 2.
.gif)
Клиническая эффективность ВТД
ВТД является важным компонентом клинических схем антихеликобактерной терапии либо в составе традиционной квадротерапии, либо в качестве дополнительного компонента тройной терапии первой линии, что дает прирост эффективности эрадикации на 15–20% [52, 53, 54]. В первую очередь, это обусловлено способностью ВТД преодолевать резистентность H. pylori к антибиотикам (особенно к кларитромицину), а не собственной бактерицидной активностью препарата висмута [55–57]. Интерес представляет также включение ВТД в схемы последовательной антихеликобактерной терапии [58].
Безопасность ВТД
Несмотря на статус тяжелого металла, висмут и его соединения считаются нетоксичными, в отличие от расположенных рядом в периодической таблице мышьяка, сурьмы, свинца и олова. Нетоксичность соединений висмута объясняется преимущественно за счет их нерастворимости в нейтральных водных растворах и биологических жидкостях и крайне низкой биодоступностью. Большинство соединений висмута являются даже менее токсичными, чем хлорид натрия [59].
A. C. Ford и соавт. в рамках метаанализа, проведенного по публикациям баз MEDLINE и EMBASE, включающего 35 рандомизированных контролируемых исследований и 4763 пациента, пришли к выводу, что терапия язвенной болезни желудка с использованием препаратов висмута безопасна и хорошо переносится. Наиболее часто встречающимся побочным эффектом является потемнение стула за счет образования сульфида висмута [60].
У очень небольшой части больных может встречаться легкое кратковременное повышение уровня трансаминаз, однако оно исчезает после окончания курса терапии. Высокие дозы ВТД, применяемые длительное время, теоретически могут быть причиной развития энцефалопатии, однако зафиксировано очень небольшое число таких поражений центральной нервной системы. Наиболее манифестное, но обратимое проявление висмутовой энцефалопатии описано у мужчины, получившего два 28-дневных курса ВТД с приемом 600 мг препарата 4 раза в день и принимавшего периодически по 240 мг/сут в течение двух лет [61].
Заключение
Уникальность ВТД состоит в том, что он сочетает в себе свойства гастропротекторного и антибактериального препарата. Его многокомпонентный механизм действия обеспечивает защиту слизистой от воздействия различных повреждающих факторов, а антихеликобактерная активность позволяет преодолевать устойчивость H. pylori к антибиотикам, повышая эффективность фармакотерапии. В общем виде совокупность отдельных компонентов механизма действия препарата представлена на рис.
_575.gif)
Новые направления создания препаратов висмута для лечения гастроэнтерологических заболеваний включают разработку висмут-содержащих наноструктур (bismuth-containing nanoparticles, Bi NPs). Так, созданный препарат нанотрубок висмута субкарбоната обладает мощным действием в отношении H. pylori (50% ингибирование в концентрации 10 мкг/мл) [62], а Bi NPs потенциально активен против грамотрицательных микроорганизмов, включая P. aeruginosa [63].
Наночастицы висмута в МИК 0,5 ммоль/л способны полностью подавлять формирование биопленки S. mutans, что сравнимо с эффектом применения хлоргексидина [64]. В работе тех же авторов водный коллоид наночастиц Bi2O3 со средним размером 77 нм эффективно угнетал рост и образование биопленок C. albicans, не проявляя цитотоксичности [65]. Делаются попытки синтеза висмут-фторхинолоновых комплексов, активных в отношении фторхинолон-резистентых штаммов микроорганизмов [66].
Исчерпывающие сведения по современным направлениям медицинской химии соединений висмута можно найти в обзоре J. A. Salvador и соавт. [67].
Литература
- Yang N., Sun H. Biological chemistry of antimony and bismuth / Biological chemistry of arsenic, antimony and bismuth/Sun H. (Ed.). Singapore: John Wiley & Sons Ltd., 2011. 400 р.
- Li W., Jin L., Zhu N. et al. Structure of collo >Postgraduate Medical Journal. 1988. Vol. 64, № 750. P. 308–310.
- Chen R., So M. H., Yang J. et al. Fabrication of bismuth subcarbonate nanotube arrays from bismuth citrate // Chem Commun. 2006. Vol. 21. P. 2265–2267.
- Pelgrift R. Y., Friedman A. J. Nanotechnology as a therapeutic tool to combat microbial resistance // Adv Drug Deliv Rev. 2013. Vol. 65, № 13–14. P. 1803–1815.
- Hernandez-Delgadillo R., Velasco-Arias D., Diaz D. et al. Zerovalent bismuth nanoparticles inhibit Streptococcus mutans growth and formation of biofilm // Int J Nanomedicine. 2012. Vol. 7. P. 2109–2113.
- Hernandez-Delgadillo R., Velasco-Arias D., Martinez-Sanmiguel J. J. et al. Bismuth oxide aqueous colloidal nanoparticles inhibit Candida albicans growth and biofilm formation // Int J Nanomedicine. 2013. Vol. 8. P. 1645–1652.
- Shaikh A. R., Giridhar R., Megraud F., Yadav M. R. Metalloantibiotics: synthesis, characterization and antimicrobial evaluation of bismuth-fluoroquinolone complexes against Helicobacter pylori. 2009. Acta Pharm. 59, 259–271.
- Salvador J. A., Figueiredo S. A., Pinto R. M., Silvestre S. M. Bismuth compounds in medicinal chemistry // Future Med Chem. 2012. Vol. 4, № 11. P. 1495–1523.
С. В. Оковитый 1 , доктор медицинских наук, профессор
Д. Ю. Ивкин, кандидат биологических наук
ГОУ ВПО СПХФА МЗ РФ, Санкт-Петербург
