| Энтероколит, вызванный Clostridium difficile | |
|---|---|
 |
|
| МКБ-10 | A 04.7 04.7. |
| МКБ-10-КМ | A04.7 |
| DiseasesDB | 2820 |
| MedlinePlus | 000259 |
| MeSH | D004761 и D004761 |
Псевдомембранозный колит — заболевание, вызывающееся спорообразующим анаэробным микробом Clostridium difficile. Несмотря на то что клинические проявления болезни весьма вариабельны, чаще всего у больных наблюдаются длительная диарея, интоксикация, боль в животе и лейкоцитоз, возникающие, как правило, на фоне антибиотикотерапии.
Содержание
Причины [ править | править код ]
Причиной псевдомембранозного энтероколита является нерациональное применение антибиотиков, приводящее к избыточному размножению определенного условно-патогенного микроба — Clostridium difficile.
Симптомы и течение [ править | править код ]
Диарея, частый водянистый стул, со слизью и кровью. Повышается температура, появляются признаки интоксикации — слабость, разбитость, тошнота, рвота. Больной жалуется на боли в животе, которые усиливаются перед дефекацией, могут быть ложные позывы, тенезмы. При объективном исследовании живот умеренно вздут, отмечается болезненность при пальпации по ходу толстой кишки. Тяжелым можно считать такое течение заболевания, когда в клинике, наряду с выраженными кишечными проявлениями, наблюдаются сердечно-сосудистые нарушения — тахикардия, гипотония; явления дегидратации и электролитные расстройства. Часто бывают признаки нарушения белкового обмена, по-видимому, вследствие экссудативной энтеропатии. Утяжеляет состояние больного развитие осложнений — перфорации кишки и токсического мегаколон. У больного с перфорацией значительно усиливаются боли, появляется локальная болезненность и напряжение мышц брюшного пресса, определяется свободная жидкость в брюшной полости, ещё более усугубляются общие расстройства.
Лечение [ править | править код ]
Первым мероприятием является отмена антибиотика, спровоцировавшего развитие псевдомембранозного колита. Этиотропная терапия заключается в назначении антибактериальных средств, к которым чувствителен Сl.difficile. Это ванкомицин и метронидазол. Ванкомицин плохо всасывается в кишечнике, при пероральном приеме его концентрация быстро нарастает. Назначается по 125 мг 4 раза в день в течение 5-7 дней. Препаратом выбора является метронидазол (0,25 3 раза в день) в течение 7-10 дней. В тяжелых случаях, когда пероральный прием затруднен, метронидазол можно назначать внутривенно. Крайне важна патогенетическая терапия, особенно у больных тяжелыми формами заболевания. Основные её направления — коррекция водно-электролитных расстройств и белкового обмена, восстановление нормального состава кишечной микрофлоры, связывание токсина Cl.difficile. Прогноз всегда серьезный.
Было показано, что ректальное введение больным людям фекалий или микроорганизмов из фекалий, взятых от здоровых доноров, вылечивает системную инфекцию Clostr >[1] [2] [3] .
Профилактика [ править | править код ]
Профилактика заболевания заключается в рациональном применении антибиотиков.
Введение
Врачи достаточно часто сталкиваются с диареей развивающейся у пациентов, на фоне или после применения антибиотиков. В России как больные, так и ряд врачей склонны связывать ее появление с «дисбактериозом». Зарубежные специалисты в этом случае говорят об «антибиотик-ассоциированной диарее». Clostridium difficile является возбудителем наиболее тяжелых форм данного осложнения, вплоть до развития фульминантного колита и токсической дилатации толстой кишки. По данным канадских исследователей уровень заболеваемости связанной с инфекцией данным возбудителем составляет от 30,8 до 40,3 случая на 100 тыс. больных (в больницах с более 200 коек) [1]. У 10 % пациентов получающих антибиотики развивается диарея, но только в 1 % случаев возникает псевдомембранозный колит.
Этиология и патогенез
Clostridium difficile это спорообразующий, анаэробный микроорганизм впервые описанный в 1935 году [7]. Однако роль токсинов Clostridium difficile в развитии псевдомембранозного колита была установлена только к 1978 году [6]. Микроорганизм далеко не всегда вызывает развитие заболевания (т.к. существуют штаммы, не продуцирующие токсины), а его тяжесть может варьировать от легкой диареи, без признаков колита, до угрожающих жизни состояний.
Патогенез заболевания включает следующие этапы
- нарушение нормальной микрофлоры толстой кишки (в норме стул содержит более 500 различных бактерий в концентрации 10 в 12 степени в одном грамме);
- колонизация толстой кишки продуцирующими токсин штаммами Clostridium difficile;
- выработка токсинов (А и В);
- воспаление и повреждение слизистой оболочки толстой кишки (до некроза эпителия и образования мембран в тяжелых случаях).
Чаще всего к развитию заболевания приводит применение клиндамицина, линкамицина, цефалоспоринов и защищенных пенициллинов [3]. Кроме недавнего (обычно не позднее 2 месяцев) применения антибиотиков риск развития инфекции повышен у лиц старше 60 лет, стационарных больных, пациентов с ослабленным иммунитетом, почечной недостаточностью, онкологическими заболеваниями и у лиц получающих антисекреторную терапию.
Клиника
К типичным симптомам данной патологии относятся диарея (стул водянистый, небольшого объема, от 4 до 20 раз в сутки, без примесей крови), схваткообразная боль в животе, а также слабость, анорексия и тошнота. Не специфическими, хотя и весьма характерными для инфекции Clostridium difficile признаками являются лейкоцитоз (до 15х109/л, а иногда и выше), гипоальбуминемия и лейкоциты в кале.
При заболевании легкой степени развивается водянистая диарея, не сопровождающаяся системными симптомами и явлениями колита при эндоскопическом обследовании.
При средней степени тяжести кроме диареи беспокоят сваткообразные боли в животе, вздутие живота, наблюдается умеренная дегидратация, тахикардия до 100 ударов в минуту, умеренный лейкоцитоз с нейтрофильным сдвигом, умеренное снижение артериального давления. При эндоскопии можно часто наблюдать характерную для псевдомембранозного колита картину.
При тяжелом течении на первое место выходят системные проявления – спутанное сознание, лихорадка, тахикардия больше 100 ударов в минуту, падение давления ниже 100 мм рт. ст., вентиляционные нарушения, высокий лейкоцитоз (до лейкемойдной реакции), развиваться токсическая делатация толстой кишки, ее перфорация, перитонит. У пациентов с таким вариантом заболевания диарея можем отсутствовать, в результате токсической дилатации толстой кишки [10].
При рентгенологическом исследовании или компьютерной томографии визуализируются «отпечатки большого пальца» свидетельствующие об отеке слизистой толстой кишки и/или дилатация толстой кишки. По данным Dallal et. al., [4] из 39 пациентов с колитом, он носил правосторонний характер у 11, левосторонний у 9 и тотальный у 19. Эндоскопическая картина может варьировать от нормы до диффузного или очагового колита с или без образования псевдомембран. Исследование не должно выполняться при подозрении на токсическую дилатацию в связи с риском перфорации толстой кишки. 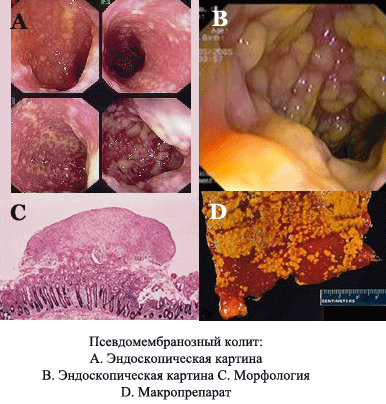
Стандартом диагностики является определение токсинов Clostridium difficile в кале. Желательно проводить определение как токсина А, так и В т.к 1-2 % штаммов Clostridium difficile продуцируют только токсин В [9]. Методика, основанная на действии цитотоксина в культуре ткани обладает высокой чувствительностью (94-100 %) и специфичностью (99 %) [10,11]. Несмотря на то, что она позволяет выявить токсин в количестве 10 pg и рассматривается в качестве «золотого стандарта» диагностики, ее проводят в немногих лабораториях, а время до получения результата занимает 24-48 часов [3].
Существует иммуноферментный метод определения токсина А и/или В в стуле. Результат исследования становиться известным в течение нескольких часов, но его чувствительность (65-85 %) и специфичность (95-100 %) ниже [2, 16]. Данный тест требует присутствия большего количества токсина для получения положительного результата (100-1000 pg) [3]. Несмотря на это, данную методику рассматривают как диагностический тест выбора у лиц с частотой стула более 6 раз в день [8]. У 5-20 % больных необходимо не однократное исследование стула для выявления токсина [14].
Получение культуры Clostridium difficile в анаэробных условиях для диагностики используется редко, во первых потому, что это занимает несколько дней, а во вторых не позволяет различить патогенные и не патогенные штаммы. Получение культуры с оценкой ее токсигенности позволяет избежать этой проблемы, но методика весьма трудоемка и занимает несколько суток.
Другие диагностические тесты включают реакцию латексной аглютенации (на клостридиальный белок глутамат дегидрогеназу, но она имеет относительно низкую чувствительность и специфичность) и определение токсинов путем полимеразной цепной реакции (находиться в процессе стандартизации).
Лечение
Одним из важнейших этапов лечения является отмена антибиотика вызвавшего заболевание (если это возможно). При легкой степени инфекции этого бывает достаточно для выздоровления [5]. При необходимости продолжения антибиотикотерапии лучше использовать препараты реже вызывающие развитие клостридиальной инфекции: аминогликозиды, сульфаниламиды, макролиды, тетрациклин и фторхинолоны.
В случае более тяжелого течения данной патологии необходимо назначение препаратов направленных на подавления Clostridium difficile. В качестве лечения выбора рассматривается Метронидазол 250 мг 4 раза в сутки или 500 мг 3 раза [15]. Ванкомицин (125 мг 4 раза в сутки) применяется при непереносимости метронидазола или его неэффективности [13]. Эффективность обеих препаратов сходна [17,18]. В обоих случаях длительность терапии 10-14 дней (улучшение состояние должно наступить в течение 72 часов). Если пациент продолжает лечение другими антибиотиками то метронидазол (ванкомицин) должен применяться весь период лечения и неделю после его прекращения [13]. Ванкомицин практически не всасывается и, следовательно, дает меньше побочных эффектов, но значительно дороже метронидазола.
Антиперистальтические агенты категорически противопоказаны. В качестве адсорбента рекомендуется холестирамин [12], но т.к. в России он отсутствует, мы с успехом вместо него используем смекту (в стандартных дозах). У пациентов с тяжелым колитом, которые не могут принимать препараты перорально, применяется метронидазол внутривенно, он выделяется в желчь и достигает достаточно высокой концентрации в просвете ЖКТ, но не ванкомицин т.к. при парентеральном введении последний в просвет ЖКТ практически не экскретируется. Впрочем, можно вводить ванкомицин (парентеральная форма) через назогастральный зонд или непосредственно в толстую кишку [13]. Не следует забывать о полноценной регидратации (пероральной или инфузионной) и коррекции электролитных нарушений.
В 10-20 % случаев при прекращении лечения возникает рецидив заболевания [19]. Он проявляется повторным возникновением симптомов через 3-21 день после прекращения применения метронидазола или ванкомицина. В таких случаях показана повторная терапия метронидазолом или ванкомицином, разумным является добавления лактобактерий и пробиотиков (хотя их эффективность не доказана).
У 0.4 %- 3,6 % пациентов требуется хирургическое лечение [13]. Наиболее частыми показаниями к операции является перитонит и токсическая дилатация толстой кишки с высоким риском перфорации. Операцией выбора является субтотальная колэктомия, но уровень летальности при ее выполнении достигает 57 % [4].
В заключение приведем схему лечения применяемую нами:
- Отмена антибиотиков (если возможно) или замена их на относительно безопасные (аминогликозиды, макролиды, фторхинолоны).
- Отмена всех антиперистальтических агентов и опиойдных анальгетиков.
- Смекта (стандартная дозировка).
- Линекс или хилак-форте (стандартная дозировка).
- Метронидазол 250 мг 4 раза в день (при системных проявлениях, частоте стула более 4 в сутки или необходимости продолжать антибиотикотерапию).
- Ванкомицин 125 мг 4 раза в сутки (при непереносимости, неэффективности метронидазола или при тяжелой инфекции).
- Метронидазол внутривенно (ванкомицин через назогастральный зонд) при невозможности самостоятельного приема препаратов.
- Коррекция водно-электролитных нарушений.
Псевдомембранозный колит — болезнь, обусловленная чрезмерным размножением Clostridium difficile, характеризуется острым началом, тяжелой диареей, гиповолемическим шоком, токсическим расширением толстой кишки, перфорацией слепой кишки, тромбогеморрагическим синдромом и без лечения приводит к гибели больного.
Этиология.Возбудители —Clostridium difficileобладают свойствами, общими и для других видов клостридий. Паразитируют в кишечнике человека. На искусственных питательных средах образуют большое количество газа и споры. Токсигенные штаммы возбудителя образуют токсин А (летальный энтеротоксин) и токсин В (цитотоксин). Около 5% здоровых людей являются носителями токсигенных клостридий. Заболевание возникает в результате бурного размноженияCl. difficile, что наблюдается при дисбактериозе, обусловленном применением антибиотиков широкого спектра действия. Клостридии чувствительны к метронидазолу и ванкомицину. Заболевание чаще развивается после применения клиндамицина, ампициллина, цефалоспоринов и аминогиликозидов. Реже возникновение заболевания связано с другими антибиотиками (исключением является ванкомицин и стрептомицин).
Эпидемиология.Заболевание чаще возникает как результат активизации эндогенной инфекции. Носителями клостридий являются здоровые люди, у 5% здоровых людей отмечается носительство токсигенных штаммов клостридий. Дети значительно чаще являются носителями токсигенных штаммов, но заболевание у них развивается реже, что связывают с наличием протективных антител, полученных от матери. Нормальная микрофлора тормозит размножение клостридий. У носителей (здоровых) при бактериологическом исследовании обнаруживаются лишь единичные колонии в расчете на 1 г испражнений, тогда как у больных псевдомембранозным колитом в 1 г испражнений содержится 10 4 –10 5 микроорганизмов. Споры клостридий устойчивы во внешней среде, и в некоторых случаях споры могут разноситься и руками медицинского персонала. В этих случаях можно говорить об экзогенной внутрибольничной инфекции. Заболевание может возникнуть иногда даже после кратковременного курса применения антибиотиков. Болезнь может возникнуть и при длительном (6 нед) применении химиопрепаратов, например, при лечении больных новообразованиями метатрексатом.
Патогенез.Псевдомембранозный колит развивается в результате воздействия токсинов, продуцируемыхCl. difficile. Выделенные от больных микробы продуцируют два токсина: токсин А — летальный энтеротоксин, обусловливающий кровоизлияния и секрецию жидкости в кишечнике, и токсин В — цитотоксин, обладающий цитопатическим эффектом в культуре ткани. В патогенезе болезни играют роль оба токсина, однако в начальный период заболевания большая роль принадлежит токсину А. Оба токсина разрушают клеточные мембраны, микрофилярии и синтез протеина. Бурное размножение клостридий и продукция ими токсинов является результатом дисбактериоза, когда антибиотики подавляют конкурентов клостридий в нормальной микрофлоре кишечника.
Симптомы и течение.Инкубационный периодпри эндогенной инфекции определить трудно. Однако если считать от начала антибиотикотерапии, то болезнь может развиться как после кратковременного курса (5–7 сут), так и после длительных (до 6 нед) курсов химиотерапии. Заболевание начинается остро. Появляется обильный, жидкий, водянистый, зеленоватого цвета стул с резким гнилостным запахом, с примесью крови. Появляются сильные схваткообразные боли в животе. Температура тела повышается до 39,5°С и выше. При пальпации отмечается спазм и болезненность кишечника. Развиваются и нарастают признаки обезвоживания (уменьшение массы тела, сухость кожи и слизистых оболочек, тахикардия, снижение АД, осиплость голоса, цианоз, судороги и др.), может развиться гиповолемический шок. В крови значительный лейкоцитоз, снижение количества альбуминов. Иногда псевдомембранозный колит протекает без поноса, что приводит к запоздалой диагностике и развитию тяжелых осложнений, таких как токсическая мегаколон и перфорация слепой кишки, что приводит к разлитому перитониту и гибели больных. В некоторых случаях в самом начале болезни, когда на фоне антибиотикотерапии появляется диарея, отмена антибиотиков может быстро привести к обратному развитию без появления характерной симптоматики.
Диагноз и дифференциальный диагноз.При распознавании псевдомембранозного колита учитывается прежде всего то, что болезнь появилась после использования антибиотиков. Клиническими особенностями является высокая лихорадка, появление водянистого стула с гнилостным запахом, развитие дегидратации, высокий лейкоцитоз. Доброкачественная неспецифическая диарея, которая может наблюдаться при антибиотикотерапии, не сопровождается лихорадкой и лейкоцитозом, самочувствие больного остается удовлетворительным.
В настоящее время хорошо отработаны диагностические критерии, позволяющие достоверно распознавать псевдомембранозный колит [R. Fekety, А. В.Shah, 1993]. Большое диагностическое значение имеет эндоскопия. В 90% случаев достаточно провести ректороманоскопию и лишь у 10% больных возникает необходимость использовать фиброколоноскопию. При ректороманоскопии выявляется гиперемия, отечность, легкая ранимость слизистой оболочки кишки. Поверхность зернистая, отмечаются геморрагии, слизистые псевдомембраны, моторика кишки повышена. Эндоскопический диагноз псевдомембранозного колита почти всегда (в 95%) удается подтвердить выделением Cl. difficile. При отсутствии псевдомембран делается биопсия слизистой оболочки кишки и при гистологическом исследовании можно обнаружить характерные изменения. При компьютерной томографии обнаруживается утолщение или диффузный отек стенки толстой кишки с явлениями периколита.
Для выделения культуры возбудителя используются селективные среды. Если данные эндоскопии не дают достаточных оснований для диагностики псевдомембранозного колита, то используется метод обнаружения в испражнениях токсина А (энтеротоксин) или токсина В (цитотоксин), продуцируемых Cl. difficile. Диагностическое значение имеет изменение течения болезни (улучшение) после отмены антибиотиков.
Дифференциальный диагнознеобходимо проводить от стафилококкового энтероколита, который также может возникать при проведении антибиотикотерапии. Он также протекает тяжело и по клиническим проявлениям может напоминать клостридиозный колит. Диагноз базируется на отрицательных результатах исследований на клостридиоз и обнаружение в стуле грамположительных кокков.
Лечение.Прежде всего необходимо прекратить антибиотикотерапию, с которой связано развитие псевдомембранозного колита, а также восстановление потерь жидкости и электролитов. У 25% больных только это мероприятие через несколько дней дает хороший результат. Если этого недостаточно, переходят к противоклостридиозной химиотерапии. Препараты назначают преимущественно пероральным путем, так какCl. difficileредко внедряются в слизистую оболочку толстой кишки. Терапевтический эффект обусловлен созданием в просвете кишки большой концентрации химиопрепарата, что прекращает продукцию токсинов и повреждения им слизистой оболочки кишки. Все штаммы возбудителя высоко чувствительны к ванкомицину и почти все — к метронидазолу.
При пероральном применении метронидазол активен как против Cl. difficile, так и по отношению к некоторым другим возбудителям острых энтероколитов. При внутривенном введении метронидазол неэффективен. Метронидазол частично всасывается в тонком кишечнике, однако и в просвете толстой кишки создается ингибирующая концентрация. Лечение легких и среднетяжелых форм начинают с назначения метронидазола (учитывают и то, что ванкомицин имеет очень неприятный вкус и в 50 раз дороже метронидазола). Метронидазол не оказывает терапевтического эффекта при стафилококковых энтероколитах.
Ванкомицинявляется предпочтительным пероральным антибиотиком для лечения тяжелых форм псевдомембранозного колита. Он является антибиотиком выбора и для лечения стафилококковых энтероколитов. Ванкомицин назначают перорально, так как при внутривенном введении он не обусловливает достаточной концентрации в просвете кишки.Сl. difficileвесьма чувствительна к ванкомицину в концентрации 16 мг/л и менее. Так как ванкомицин не всасывается в желудочно-кишечном тракте, то при пероральном назначении в дозах 0,5–2 г/сут (разделить на 3–4 приема) создается концентрация в испражнениях 500–2000 мг/л. Даже относительно небольшие дозы ванкомицина (125–250 мг 4 раза в день) дают достаточно высокую концентрацию в стуле даже при наличии у больного профузного поноса. При назначении ванкомицина выраженное улучшение отмечается уже через 3–4 дня. Для подавления возбудителя и прекращения продукции токсинов достаточно 10-дневного курса лечения. После курса лечения могут некоторое время сохраняться повышение температуры тела и понос как результат еще незакончившегося воспалительного процесса в толстой кишке. Очень неприятный (горький) вкус ванкомицина может быть преодолен при использовании капсул, введения ванкомицина через назогастральный зонд или в клизме (через длинную трубку).
У 10–20 % больных через 1–4 нед после окончания лечения наступают рецидивы псевдомембранозного колита за счет сохранившихся в кишечнике спор или в результате нового заражения. Рецидивы хорошо поддаются терапии метронидазолом и ванкомицином, если лечение начать рано. При многократных рецидивах применяют длительный курс лечения ванкомицином (4–6 нед) или несколько 5–7-дневных курсов с перерывами между ними. Используют бактериальные препараты для восстановления нормальной микрофлоры кишечника.
Прогноз.При легких и среднетяжелых формах прогноз благоприятный. При тяжелых осложненных формах (токсическое расширение толстой кишки, непроходимость кишечника, перфорация слепой кишки) летальность достигает 30%.
Профилактика и мероприятия в очаге.Рациональная антибиотикотерапия, ранняя диагностика и лечение больных. Комплекс мер для предупреждения инфекций с фекально-оральным механизмом передачи. Специфическая профилактика не разработана.
