Брюшной тиф и паратифыА и В— острые кишечные инфекции, характеризующиеся поражением лимфатического аппарата кишечника, выраженной интоксикацией. Их возбудителями являются соответственно Salmonella typhi, Salmonella paratyphi А и Salmonella schottmuelleri.
Таксономическое положение. Возбудители брюшного тифа и паратифов А и В относятся к отделу Gracilicutes, семейству Enterobacteriaceae, роду Salmonella.
Морфологические и тинкториальные свойства. Сальмонеллы — мелкие грамотрицательные палочки с закругленными концами. В мазках располагаются беспорядочно. Не образуют спор, имеют микрокапсулу, перитрихи.
Культуральные свойства. Сальмонеллы — факультативные анаэробы. Оптимальными для роста являются температура 37С. Растут на простых питательных средах. Элективной средой для сальмонелл является желчный бульон.
Биохимическая активностьсальмонелл достаточно высока, но они не сбраживают лактозу. S.typhi менее активна, чем возбудители паратифов.
Антигенные свойства и классификация. Сальмонеллы имеют О— и H-антигены, состоящие из ряда фракций. Каждый вид обладает определенным набором антигенов. Все виды сальмонелл, имеющие общую так называемую групповую фракцию 0-антигена, объединены в одну группу. Таких групп в настоящее время насчитывается около 65. S.typhi и некоторые другие сальмонеллы имеют Vi-антиген (разновидность К-антигена), с этим антигеном связывают вирулентность бактерий, их устойчивость к фагоцитозу.
Факторы патогенности. Сальмонеллы образуют эндотоксин, обладающий энтеротропным, нейротропным и пирогенным действием. С белками наружной мембраны связаны адгезивные свойства, наличие микрокапсулы обусловливает устойчивость к фагоцитозу.
Резистентность. Сальмонеллы довольно устойчивы к низкой т-ре. Очень чувствительны к дезинфицирующим веществам, высокой температуре, ультрафиолетовым лучам. В пищевых продуктах (мясе, молоке) сальмонеллы могут не только долго сохраняться, но и размножаться.
Эпидемиология. Брюшной тиф и паратиф А — антропонозные инфекции; источником заболевания являются больные люди и бактерионосители. Источником паратифа В могут быть также сельскохозяйственные животные. Механизм заражения фекально-оральный. Среди путей передачи преобладает водный.
Патогенез. Возбудители попадают в организм через рот, достигают тонкой кишки, где в ее лимфатических образованиях размножаются и затем попадают в кровь (стадия бактериемии). С током крови они разносятся по всему организму, внедряясь в паренхиматозные органы (селезенку, печень, почки, костный мозг). При гибели бактерий освобождается эндотоксин, вызывающий интоксикацию. Из желчного пузыря, где С. могут длительно сохраняться, они вновь попадают в те же лимфатические образования тонкой кишки. В результате повторного поступления С. может развиться аллергическая реакция, проявляющаяся в виде воспаления, а затем некроза лимфатических образований. Сальмонеллы выводятся из организма с мочой и калом.
Клиника. Клинически брюшной тиф и паратифы неразличимы. Инкубационный период составляет 12 дней. Болезнь начинается остро: с повышения температуры тела, появления слабости, утомляемости; нарушаются сон и аппетит. Для брюшного тифа характерны помутнение сознания, бред, галлюцинации, сыпь. Очень тяжелыми осложнениями являются прободение стенки кишки, перитонит, кишечное кровотечение, возникающие в результате некроза лимфатических образований тонкой кишки.
Иммунитет. После перенесенной болезни иммунитет прочный и продолжительный.
Микробиологическая диагностика.Основной метод диагностики — бактериологический: посев и выделение S. typhi из крови (гемокультура), фекалий (копрокультура), мочи (урино-культура), желчи, костного мозга. РИФ для обнаружения антигена возбудителя в биологических жидкостях. Серологический метод обнаружения 0- и Н- антител в РПГА. Бактерионосителей выявляют по обнаружению Vi-антител в сыворотке крови с помощью РПГА и положительному результату бактериологического; выделения возбудителя. Для внутривидовой идентификации применяют фаготипирование.
Лечение. Антибиотики. Иммуноантибиотикотерапия.
Профилактика. Санитарно-гигиенические мероприятия. Вакцинация — брюшнотифозная химическая и брюшно-тифозная спиртовая вакцина, обогащенная Vi-антигеном. Для экстренной профилактики — брюшнотифозный бактериофаг.
• Билет№9
• Структура и химический состав вирусов и бактериофагов
Вирусы— мельчайшие микробы, не имеющие клеточного строения, белоксинтезирующей системы, содержащие только ДНК или РНК. Относятся к царству Vira. Являясь облигатными внутриклеточными паразитами, вирусы размножаются в цитоплазме или ядре клетки. Они — автономные генетические структуры. Отличаются особым — разобщенным (дисъюнктивным) способом размножения (репродукции): в клетке отдельно синтезируются нуклеиновые кислоты вирусов и их белки, затем происходит их сборка в вирусные частицы. Сформированная вирусная частица называется вирионом.Бактериофа́ги — вирусы, избирательно поражающие бактериальные клетки. Чаще всего бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило, бактериофаг состоит из белковой оболочки и генетического материала одноцепочечной или двуцепочечной нуклеиновой кислоты (ДНК или, реже, РНК). Размер частиц приблизительно от 20 до 200 нм.
Морфологию и структуру вирусов изучают с помощью электронного микроскопа, так как их размеры малы и сравнимы с толщиной оболочки бактерий.
Форма вирионов может быть различной: палочковидной (вирус табачной мозаики), пулевидной (вирус бешенства), сферической (вирусы полиомиелита, ВИЧ), в виде сперматозоида (многие бактериофаги). Различают просто устроенные и сложно устроенные вирусы.
Простые, или безоболочечные, вирусысостоят из нуклеиновой кислоты и белковой оболочки, называемой капсидом. Капсид состоит из повторяющихся морфологических субъединиц — капсомеров. Нуклеиновая кислота и капсид взаимодействуют друг с другом, образуя нуклеокапсид.
Сложные, или оболочечные, вирусыснаружи капсида окружены ли-попротеиновой оболочкой (суперкапсидом, или пеплосом). Эта оболочка является производной структурой от мембран вирус-инфицированной клетки. На оболочке вируса расположены гликопротеиновые шипы, или шипики (пепломеры). Под оболочкой некоторых вирусов находится матриксный М-белок.
Капсид и суперкапсид защищают вирионы от влияния окружающей среды, обусловливают избирательное взаимодействие (адсорбцию) с клетками, определяют антигенные и иммуногенные свойства вирионов. Внутренние структуры вирусов называются сердцевиной.
Тип симметрии. Капсид или нуклеокапсид могут иметь спиральный, икосаэдрический (кубический) или сложный тип симметрии. Икосаэдрический тип симметрии обусловлен образованием изометрически полого тела из капсида, содержащего вирусную нуклеиновую кислоту (например, у вирусов гепатита А, герпеса, полиомиелита). Спиральный тип симметрии обусловлен винтообразной структурой нуклеокапсида (например, у вируса гриппа).
Включения— скопление вирионов или отдельных их компонентов в цитоплазме или ядре клеток, выявляемые под микроскопом при специальном окрашивании. Вирус натуральной оспы образует цитоплазмати-ческие включения — тельца Гварниери; вирусы герпеса и аденовирусы — внутриядерные включения.
Размеры вирусов определяют с помощью электронной микроскопии, методом ультрафильтрации через фильтры с известным диаметром пор, методом ультрацентрифугирования. Одним из самых мелких вирусов является вирус полиомиелита (около 20 нм), наиболее крупным — натуральной оспы (около 350 нм).
Вирусы имеют уникальный геном, так как содержат либо ДНК, либо РНК. Поэтому различают ДНК-содержащие и РНК-содержащие вирусы. Они обычно гаплоидны, т.е. имеют один набор генов. Геном вирусов представлен различными видами нуклеиновых кислот: двунитчатыми, однонитчатыми, линейными, кольцевыми, фрагментированными. Среди РНК-содержащих вирусов различают вирусы с положительным (плюс-нить РНК) геномом. Плюс-нить РНК этих вирусов выполняет наследственную функцию и функцию информационной РНК (иРНК). Имеются также РНК-содержащие вирусы с отрицательным (минус-нить РНК) геномом. Минус-нить РНК этих вирусов выполняет только наследственную функцию.
Геном вирусов способен включаться в состав генетического аппарата клетки в виде провируса, проявляя себя генетическим паразитом клетки. Нуклеиновые кислоты некоторых вирусов (вирусы герпеса и др.) могут находиться в цитоплазме инфицированных клеток, напоминая плазмиды.
• Иммуноферментный анализ, иммуноблоттинг.
Иммуноферментный анализили метод — выявление антигенов с помощью соответствующих им антител, конъюгированных с ферментом-меткой (пероксидазой хрена, бета-галактозидазой или щелочной фосфатазой). После соединения антигена с меченной ферментом иммунной сывороткой в смесь добавляют субстрат/хромоген. Субстрат расщепляется ферментом и изменяется цвет продукта реакции — интенсивность окраски прямо пропорциональна количеству связавшихся молекул антигена и антител. ИФА применяют для диагностики вирусных, бактериальных и паразитарных болезней, в частности для диагностики ВИЧ-инфекций, гепатита В и др., а также определения гормонов, ферментов, лекарственных препаратов и других биологически активных веществ, содержащихся в исследуемом материале в минорных концентрациях (10 10 -10 12 г/л). Твердофазный ИФА— вариант теста, когда один из компонентов иммунной реакции (антиген или антитело) сорбирован на твердом носителе, напр., в лунках планшеток из полистирола. Компоненты выявляют добавлением меченых антител или антигенов. При положительном результате изменяется цвет хромогена. Каждый раз после добавления очередного компонента из лунок удаляют несвязавшиеся реагенты путем промывания,
I. При определении антител (левый рисунок) в лунки планшеток с сорбированным антигеном последовательно добавляют сыворотку крови больного, антиглобулиновую сыворотку, меченную ферментом, и субстрат/хромоген для фермента.
II. При определении антигена в лунки с сорбированными антителами вносят антиген (сыворотку крови с искомым антигеном), добавляют диагностическую сыворотку против него и вторичные антитела (против диагностической сыворотки), меченные ферментом, а затем субстрат/хромоген для фермента.
Конкурентный ИФАдля определения антигенов: искомый антиген и меченный ферментом антиген конкурируют друг с другом за связывание ограниченного количества антител иммунной сыворотки.
Другой тест — Конкурентный ИФА для определения антител: искомые антитела и меченные ферментом антитела конкурируют друг с другом за антигены, сорбированные на твердой фазе.
Иммуноблоттинг — высокочувствительный метод выявления белков, основанный на сочетании электрофореза и ИФА или РИА. Иммуноблоттинг используют как диагностический метод при ВИЧ-инфекции и др.
Антигены возбудителя разделяют с помощью электрофореза в полиакриламидном геле, затем переносят их из геля на активированную бумагуили нитроцеллюлозную мембрану и проявляют с помощью ИФА. Фирмы выпускают такие полоски с «блотами» антигенов. На эти полоски наносят сыворотку больного. Затем, после инкубации, отмывают от несвязавшихся антител больного и наносят сыворотку против иммуноглобулинов человека, меченную ферментом. Образовавшийся на полоске комплекс [антиген + антитело больного + антитело против Ig человека] выявляют добавлением хромогенного субстрата, изменяющего окраску под действием фермента.
• ВИЧ-инфекция. Таксономия, характеристика
Вирус иммунодефицита человека вызывает ВИЧ-инфекцию, заканчивающуюся развитием синдрома приобретенного иммунного дефицита.
Возбудитель ВИЧ-инфекции — лимфотропный вирус, относящийся к семейству Retroviridae роду Lentivirus.
Морфологические свойства:РНК-содержащий вирус. Вирусная частица сферической формы Оболочка состоит из двойного слоя липидов, пронизанного гликопротеинами. Липидная оболочка происходит из плазматической мембраны клетки хозяина, в которой репродуцируется вирус. Гликопротеиновая молекула состоит из 2 субъединиц, находящихся на поверхности вириона и пронизывающих его липидную оболочку.
Сердцевина вируса конусовидной формы, состоит из капсидных белков, ряда матриксных белков и белков протеазы. Геном образует две нити РНК, для осуществления процесса репродукции ВИЧ имеет обратную транскриптазу, или ревертазу.
Геном вируса состоит из 3 основных структурных генов и 7 регуляторных и функциональных генов. Функциональные гены выполняют регуляторные функции и обеспечивают осуществление процессов репродукции и участие вируса в инфекционном процессе.
Вирус поражает в основном Т- и В-лимфоциты, некоторые клетки моноцитарного ряда (макрофаги, лейкоциты), клетки нервной системы. Культуральные свойства: на культуре клеток Т-лимфоцитов и моноцитов человека (в присутствии ИЛ-2). Антигенная структура:2 типа вируса — ВИЧ-1 и ВИЧ-2 ВИЧ-1, имеет более 10 генотипов (субтипов): А, В, С, D, E, F…, отличающихся между собой по аминокислотному составу белков.
ВИЧ-1 делят на 3 группы: М, N, О. Большинство изолятов относится к группе М, в которой выделяют 10 подтипов: А, В, С, D, F-l, F-2, G, Н, I, К. Устойчивость:Чувствителен к физическим и химическим факторам, гибнет в при нагревании. Вирус может длительно сохраняться в высушенном состоянии, в высохшей крови.
Факторы патогенности, патогенез: Вирус прикрепляется к лимфоциту, проникает в клетку и репродуцирует в лимфоците. В результате размножения ВИЧ в лимфоците последние разрушаются или теряют свои функциональные свойства. В результате размножения вируса в различных клетках происходит накопление его в органах и тканях, и он обнаруживается в крови, лимфе, слюне, моче, поте, каловых массах.
При ВИЧ-инфекции снижается число Т-4-лимфоцитов, нарушается функция В-лимфоцитов, подавляется функция естественных киллеров и ответ на антигены снижается и нарушается продукция комплемента, лимфокинов и других факторов, регулирующих иммунные функции (ИЛ), в результате чего наступает дисфункция иммунной системы.
Клиника: поражается дыхательная система (пневмония, бронхиты); ЦНС (абсцессы, менингиты); ЖКТ (диареи), возникают злокачественные новообразования (опухоли внутренних органов).
ВИЧ-инфекция протекает в несколько стадий: 1) инкубационный период, составляющий в среднем 2—4 недели; 2) стадия первичных проявлений, характеризующаяся вначале острой лихорадкой, диареей; завершается стадия бессимптомной фазой и персистенцией вируса, восстановлением самочувствия, однако в крови определяются ВИЧ-антитела, 3) стадия вторичных заболеваний, проявляющихся поражением дыхательной, нервной системы. Завешается ВИЧ-инфекция последней, 4-й терминальной стадией- СПИДом.

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
| Брюшной тиф | |
|---|---|
 Фотография микропрепарата Salmonella enterica |
|
| МКБ-10 | A 01.0 01.0 |
| МКБ-10-КМ | A01.0 и A01.00 |
| МКБ-9 | 002 002 |
| МКБ-9-КМ | 002.0 [1] [2] |
| DiseasesDB | 27829 |
| MedlinePlus | 001332 |
| eMedicine | oph/686 med/2331 med/2331 |
| MeSH | D014435 |
Брюшной тиф — острая циклически протекающая кишечная антропонозная инфекция, вызываемая бактериями Salmonella typhi (Salmonella enterica серотип typhi) [3] , с алиментарным путём передачи, характеризующаяся лихорадкой, явлениями общей интоксикации с развитием тифозного статуса, розеолезными высыпаниями на коже, гепато- и спленомегалией и специфическим поражением лимфатической системы нижнего отдела тонкой кишки [4] .
Одной из первых исторически известных эпидемий брюшного тифа была Афинская чума [5] .
В России (XIX в.) брюшной тиф был известен как «горячка с пятнами» [6] .
В 2000 году брюшным тифом в мире переболели 21,6 млн человек, из них около 1 % с летальным исходом [7] .
Содержание
Этиология [ править | править код ]
, 96 % этилового спирта они гибнут через несколько минут [10] .</p>
<h2><span class=)

Период заразительности источника. Наибольшее выделение возбудителя с фекалиями наблюдается в течение 1-5 нед заболевания с максимумом на 3-й нед, с мочой — в течение 2-4 нед. Реконвалесценты нередко выделяют возбудителя во внешнюю среду в течение 14 дней (транзиторное носительство), у 10 % переболевших этот процесс продолжается до 3 мес. (острое носительство), а 3-5 % становятся хроническими носителями, выделяя брюшнотифозную палочку в течение ряда лет. Перемежающийся характер выделения возбудителя брюшного тифа у хронических носителей затрудняет выделение и повышает их эпидемиологическую опасность.
Механизм передачи возбудителя фекально-оральный. Путь передачи — преимущественно водный, но возможны пищевой (кефир, сметана, молоко, йогурт, фарш и тд) и бытовой пути передачи.
Естественная восприимчивость людей высокая, хотя клинические проявления заболевания могут варьироваться от стертых до тяжело протекающих форм. Перенесённое заболевание оставляет стойкий иммунитет.
Основные эпидемиологические признаки. Болезнь имеет убиквитарное распространение, однако заболеваемость преобладает на территориях с неблагополучными водоснабжением и канализацией. При водных вспышках чаще поражаются подростки и взрослые, при молочных — дети младшего возраста. Характерна летне-осенняя сезонность.
Клиническая картина [ править | править код ]
Инкубационный период — от 7 дней до 23 дней, в среднем 2 нед. Возбудитель — рот — кишечник — пейеровы бляшки и солитарные фолликулы (лимфаденит и лимфангит) — кровяное русло — бактериемия — первые клинические проявления. Циркулирующие в крови микроорганизмы частично погибают — высвобождается эндотоксин, обусловливающий интоксикационный синдром, а при массивной эндотоксемии — инфекционно-токсический шок.
Начальный период (время от момента появления лихорадки до установления её постоянного типа) — продолжается 4-7 дней и характеризуется нарастающими симптомами интоксикации. Бледность кожи, слабость, головная боль, снижение аппетита, брадикардия. Обложенность языка белым налётом, запоры, метеоризм, поносы.
Период разгара — 9-10 дней. Температура тела держится постоянно на высоком уровне. Симптомы интоксикации резко выражены. Больные заторможены, негативны к окружающему. При осмотре на бледном фоне кожи можно обнаружить бледно-розовые единичные элементы сыпи — розеолы, слегка выступающие над поверхностью кожи, исчезающие при надавливании, располагающиеся на коже верхних отделов живота, нижних отделов грудной клетки, боковых поверхностях туловища, сгибательных поверхностях верхних конечностей. Отмечаются глухость тонов сердца, брадикардия, гипотония. Язык обложен коричневатым налётом, с отпечатками зубов по краям. Живот вздут, имеется склонность к запорам. Увеличивается печень и селезёнка. Тифозный статус — резкая заторможенность, нарушение сознания, бред, галлюцинации. Другим проявлением тяжести болезни является инфекционно-токсический шок.
Период разрешения болезни. Температура падает критически или ускоренным лизисом, уменьшается интоксикация — появляется аппетит, нормализуется сон, постепенно исчезает слабость, улучшается самочувствие.
В период реконвалесценции у 3-10 % больных может наступить рецидив болезни. Предвестниками рецидива являются субфебрилитет, отсутствие нормализации размеров печени и селезёнки, сниженный аппетит, продолжающаяся слабость, недомогание. Рецидив сопровождается теми же клиническими проявлениями, что и основная болезнь, но протекает менее продолжительно.
Брюшной тиф может протекать в легкой, среднетяжелой и тяжелой формах. Выделяют атипичные формы болезни — абортивные и стертые.
В настоящее время в клинической картине брюшного тифа произошли большие изменения. Это связано с повсеместным применением антибиотиков, а также с иммунопрофилактикой. Вследствие этого стали преобладать стертые и абортивные формы заболевания. Лихорадка может длиться до 5-7 дней (иногда 2-3 дня). Чаще встречается острое начало (без продромального периода — в 60-80% случаев). Что касается картины крови, то в 50% случаев сохраняется нормоцитоз, эозинофилы в норме. Серологические реакции на брюшной тиф могут быть отрицательными в течение всей болезни.
Диагностика [ править | править код ]
Лабораторная диагностика прежде всего заключается в бактериологическом исследовании крови, кала, мочи, желчи. Метод гемокультуры можно использовать с первых дней заболевания и до конца лихорадочного периода, желательно до начала лечения. Для этого 5-10 мл крови из локтевой вены у постели больного засевают на 20 % желчный бульон или среду Рапопорта, мясопептонный бульон с 1 % глюкозы, либо даже в стерильную дистиллированную воду. Объем среды — 50-100 мл. Соотношение материала и среды должно быть 1:10. Кал, мочу, дуоденальное содержимое исследуют со 2-й недели от начала заболевания, засевая на среды Плоскирева, Левина, Мюллера и др. Предварительный результат этих исследований получают через 2 дня, окончательный — через 4 дня.
Для выявления брюшной тифозной палочки в фекалиях, моче, дуоденальном содержимом используют РИФ с меченными сыворотками к О- и Vi-антигенам. Предварительный ответ может быть получен в течение 1 ч, окончательный — через 5-20 ч.
Из серологических методов используют РА (Видаля) и РПГА с цистеином. Реакцию Видаля ставят с Н- и О-антигенами с 7-9-го дня заболевания повторяют на 3-4-й неделе для определения нарастания титра (от 1:200 до 1:400-1:800-1:1600). Последнее имеет значение для исключения положительного результата реакции, который может быть обусловлен предшествовавшей иммунизации против брюшного тифа. Ответ может быть получен через 18-20 ч. При постановке РПГА учёт результатов проводят после инкубирования пластин при 37° С в течение 1,5-2 ч и повторно — через 24 ч нахождения при комнатной температуре. Положительный считается реакция в титре 1:40 и выше.
Лечение [ править | править код ]

Госпитализация. Режим в остром периоде и до 10-го дня нормальной температуры тела постельный, а при осложнениях — строгий постельный. Расширение режима — с осторожностью: не производить резких движений, не поднимать тяжестей, не натуживаться во время дефекации.
Резкое ограничение механических и химических раздражителей слизистой оболочки желудочно-кишечного тракта, исключение продуктов и блюд, усиливающих процессы брожения и гниения в кишечнике. При неосложненных формах стол № 4а бт, за 5—7 дней до выписки замена на № 15. Приём комплекса витаминов (аскорбиновая кислота — до 900 мг/сут, витамины В1 и В2 по 9 мг, РР — 60 мг, Р — 300 мг/сут).
Курс терапии до 10-го дня нормальной температуры тела вне зависимости от тяжести течения и быстроты клинического выздоровления больного. Если в течение 4—5 дней нет перелома в состоянии — отменить и назначить другой.
Левомицетин (хлорамфеникол). взрослым внутрь за 20—30 мин до еды 50 мг/кг/сут, на 4 приёма. После нормализации температуры тела − 30 мг/кг/сут. В случаях невозможности перорального приёма (тошнота, рвота, боли в эпигастрии) парентерально — левомицетина сукцината 3 г в сутки или ампициллин: взрослым внутрь после еды по 1—1,5 г 4—6 р/с или парентерально 6 г/с. триметоприма (80 мг в таблетках) и сульфаметоксазола (400 мг в таблетках) — бисептола, бактрима, септрина, котримоксазола. взрослым внутрь по 2 таблетки 2 р/д после еды (при тяжелых формах 3 таб) 3—4 недели.
Лечение тяжелых, осложнённых и сочетанных форм эффективно парентерально комбинации ампициллина (6—8 г/сут) и гентамицина (240 мг/сут). Для дезинтоксикации в легких случаях обильное питьё (до 2,5—3 л в сутки), энтеросорбенты через 2 часа после еды (энтеродез — 15 г/сут, полифепан — 75 г/сут, угольные сорбенты — 90 г/сут) и ингаляции кислорода через носовые катетеры по 45—60 мин 3—4 раза в сутки.
При среднетяжелом течении дезинтоксикация + парентеральным введением изотонических глюкозо-солевых растворов до 1,2—1,6 л/сут (5 % раствор глюкозы, лактасол, квартасол, ацесоль, хлосоль), 5—10 % раствора альбумина по 250—100 мл, бензонала натрия по 0,1 г внутрь 3 раза в день (за счёт стимуляции микросомальных ферментов печени). При нарастании интоксикации показано назначение преднизолона (45—60 мг в сутки) перорально коротким курсом (5—7 дней), проведение курса оксигенобаротерапии. В тех случаях, когда проводимая терапия не даёт положительных результатов в течение 3 суток, при микст-инфекциях и рецидивах заболевания в комплексе лечебных мероприятий показана гемосорбция и переливание крови.
Всем больным брюшным тифом и паратифами назначаются стимуляторы лейкопоэза и репаративных процессов (метилурацил по 0,5 г или пентоксил по 0,3 г 3 раза в день после еды), ангиопротекторы (аскорутин по 1 таблетке 3 раза в день). В периоде реконвалесценции лицам с выраженной астенизацией показаны адаптагены — настойка элеутерококка, заманихи, корня женьшеня, пантокрина, лимонника китайского в обычных терапевтических дозировках.
Энтеросорбция при брюшном тифе [ править | править код ]
Сложившаяся система лечения брюшного тифа не вполне удовлетворяет клиницистов, так как интоксикация при этом заболевании остается весьма выраженной, этиотропное же лечение недостаточно эффективно. Исходя из этого применение энтеросорбентов при тифо-паратифозных заболеваниях является оправданным. [11]
Диспансерное наблюдение за переболевшими [ править | править код ]
Прекращение бактериовыделения бывает временным и через некоторое время (до нескольких лет) может возобновляться. Выписка реконвалесцентов осуществляется на фоне полного клинического выздоровления, нормализации лабораторных показателей, после 3-кратных отрицательных посевов кала, мочи и однократного—желчи, но не ранее 21-го дня нормальной температуры тела. После выписки из стационара переболевшие подлежат диспансерному наблюдению, по истечении 3 мес проводится бактериологическое исследование кала, мочи и желчи. При отрицательных результатах наблюдение прекращается. Реконвалесценты из числа работников пищевых и приравненных к ним предприятий находятся под наблюдением на протяжении всей трудовой деятельности. В XX веке было известно несколько очагов заболеваний, вызванных бессимптомными носителями, одними из самых известных которых были так называемые Тифозная Мэри и Тифозный Джон.
Возбудители брюшного тифа, паратифов
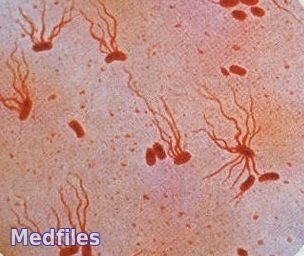
Возбудителя брюшного тифа (S. typhi) выявил впервые немецкий гистолог Эберт в 1880 г., увидевший его при микроскопии гистологических препаратов – срезов селезенки, периферических лимфоузлов и пейеровых бляшек, взятых у умерших от тифа больных. В 1884 г. Гаффки получил чистую культуру возбудителя. В этом же году А. Брион и Х. Кайзер описали возбудителя паратифа А (S. paratyphi A), а Г. Шоттмюллер – возбудителя паратифа В (S. paratyphi В). Этих сальмонелл выделили в чистой культуре и изучили Ашар и Бедсон в 1896 г.
Родовое название связано с именем американского ветеринарного врача Д. Сальмона, который в 1885 г. выделил возбудителя сальмонеллезов (S. choleraesuis) от больных свиней. В 1888 г. Гертнер выделил S. enteritidis из мяса и селезенки коров, погибших от острой пищевой инфекции. В 1890 г. Леффлер, 1893 г. С.С. Мережковский и 1900 г. Даниш обнаружили другого возбудителя S. typhimurium, вызвавшего аналогичные заболевания у человека и у мышей.
В 1934 г. Ф. Кауфман и П. Уайт разработали классификацию сальмонелл по антигенной структуре.
(вызывают заболевания у человека и животных)
S. typhi (палочка Эберта-Гаффки)
S. paratyphi A (палочка Бриона-Кайзера)
S. paratyphi В (палочка Шоттмюллера)
Однако в большинстве учебных пособий и справочников для удобства используется исторически сложившаяся таксономия, рассматривающая серовары, как виды (например, S . typhi , вместо S . enterica подвид enterica серовар Typhi )
Морфология и тинкториальные свойства.
Мелкие грамотрицательные палочки с закругленными концами размером 0,7-1,5?2-5 мкм, в мазках располагаются беспорядочно, подвижны (перетрихи), имеют пили I и II типов, S . typhi – микрокапсулу, спор не образуют.
Факультативные анаэробы, хемоорганогетеротрофы. Не требовательны к условиям культивирования: оптимальная температура роста 370С, значение рН 6,8-7,2, длительность культивирования – 24-48 часа. Хорошо растут на простых питательных средах (МПБ, МПА). В МПБ наблюдается рост в виде диффузного помутнения с последующим образованием осадка. На МПА образуют колонии в S — (средних размеров, гладкие, блестящие, полупрозрачные с голубоватым оттенком) и R -форме, S . paratyphi В и S . enteritidis по краю колоний формируют слизистый валик. В качестве накопительных сред используют желчный и селенитовый бульон. На дифференциально- диагностических средах Эндо, Левина и Плоскирева образуют бесцветные колонии (не ферментируют лактозу). На висмут-сульфитном агаре – колонии черного цвета с металлическим блеском, окруженные черным ободком прокрашенной среды.
Сальмонеллы обладают выраженной ферментативной активностью. Оксидазоотрицательны и каталазоположительны. Реакция Фогеса-Проскауэра отрицательная. Сахаролитическая активность: не расщепляют лактозу и сахарозу; глюкозу, маннит, мальтозу и другие сахара разлагают до кислоты и газа (исключение, S . typhi – до кислоты), по способности разлагать ксилозу и арабинозу различают 4 типа: К+А+; К-А-; К+А-; К-А+. Протеолитические свойства: не образуют индол, желатин не разжижают, образуют H 2 S (исключение, S . paratyphi A ).
Антигенная структура сальмонелл – сложная, имеются О-, Н-, Vi -, М-антигены.
* О – соматический антиген, липополисахарид клеточной стенки, термостабильный, (выдерживает кипячение в течение 2,5 часов, автоклавирование при 1200 С – 30 мин.), чувствительны к формальдегиду, но устойчив к спирту, групповой – согласно классификации Кауфмана-Уайта, семейство делится на 67 серогрупп (А, В, С, Д…). О-АГ состоит из R -ядра и боковой S -цепи, к которой присоединяются сахара – рецепторы (обозначаются цифрами). Общность конечного сахара (по химической природе является 3,6-дидезоксигексозой) является основанием для объединения в серогруппу. Некоторые группы имеют общие О-АГ, но каждая группа содержит один основной антиген: в группе А – 2, в группе В – 4, в группе С – 7, Д – 9…
* Н – жгутиковый антиген, белок флагеллин, термолабильный (разрушается при нагревании до 75-100С, а также под действием соляной кислоты, спирта, протеолитических ферментов), типовой (более 250 сероваров, расположены в алфавитном порядке в таблице Кауфмана-Уайта). У Н-АГ сальмонелл различают 2 фазы: I (специфическая) – различна у серотипов, входящих в одну группу, обозначается строчными латинскими буквами; II (неспецифическая) – содержат в своем составе общие для всей группы компоненты, обозначается арабскими цифрами. Если у серовара присутствуют обе фазы Н-АГ, то его называют двухфазным, если одна – монофазным.
* Vi -АГ – поверхностный полисахаридный антиген S . typhi , являющийся разновидностью К-АГ, термолабильный (разрушается при кипячении за 10 минут), чувствительный к соляной кислоте и спирту, встречается только у вирулентных сальмонелл, препятствует агглютинации О-антисыворотками, является рецептором для бактериофагов.
* М-АГ – слизистый, водонерастворимый, разрушается под действием кислот и спиртов.
* эндотоксин – липополисахарид клеточной стенки, высвобождается при массовой гибели возбудителей, играет основную роль в патогенезе брюшного тифа, оказывая пирогенное и токсическое действие;
* возбудители сальмонеллезов выделят экзотоксины – термолабильный белковый энтеротоксин, сходный с холерогеном и LT -токсином E . coli (увеличивают в клетках эпителия тонкого кишечника содержание цАМФ, что приводит к повышенному выходу воды из клеток и развитию диареи) + цитотоксическое действие, вызывая гибель энтероцитов.
2. Ферменты патогенности: гиалуронидаза, фибринолизин, лецитиназа, муциназа, протеаза, супероксиддисмутаза (инактивирует суперактивные радикалы О2, что придает устойчивость к фагоцитозу).
3. Структурные и химические компоненты клетки:
* пили I и II типов;
* микрокапсула у S . typhi ;
* белки наружной мембраны – инвазины (обеспечивающие инвазию слизистой и резистентность к фагоцитозу, позволяющую сальмонеллам сохраняться и размножаться внутри фагоцитов);
Резистентность у сальмонелл – достаточно высокая. Выдерживают рН в диапозоне 4-9, в водоемах, сточных водах, почве сохраняют жизнеспособность до 3 месяца, в комнатной пыли – от 80 до 550 дней. Хорошо переносят низкие температуры: во льду сохраняются более 60 дней, в замороженном мясе – 6-13 месяцев (в толще мяса могут сохраняться и после тепловой обработки), размножается в мясном фарше при +50С, в яйцах – до 13 месяцев (при хранении яиц в холодильнике могут проникать через неповрежденную скорлупу и размножаться в желтке), в колбасе – 2-4 месяца, в хлебе – до 3-х месяцев, на овощах и фруктах – 5-10 дней. Хуже выдерживают высокую температуру: при 560 С выдерживают 40-60 минут, при 700 С погибают через 10 минут, при 1000 С – моментально. Чувствительны к дезрастворам в рабочей концентрации (5% фенол, 3% хлорамин, 3% лизол вызывают гибель бактерий через 2-3 минуты) и антибиотикам.
Брюшной тиф (название болезни дал Гиппократ, происходит от греч. typos – туман, спутанное сознание) – острое антропонозное инфекционное заболевание, характеризующееся поражением лимфоидного аппарата тонкого кишечника, бактериемией, выраженной лихорадкой, интоксикацией и розеолезной сыпью. Паратифы А и В сходны по характеру и клиническим проявлениям с брюшным тифом, но протекают более легко.
Сальмонеллезы – группа полиэтиологичных острых зооантропонозных кишечных инфекций, протекающих по типу гастроэнтеритов у взрослых и токсико-септических инфекций у детей.
Источник инфекции: больные и бактерионосители.
Механизм передачи: фекально-оральный (пути: пищевой, водный, контактно-бытовой). Брюшной тиф и паратиф А распространяются чаще водным путем (употребление воды из неглубоких загрязненных водоемов, технических водопроводов, в случаях прорыва канализационных вод). При паратифе В преобладает пищевой путь (заражение чаще происходит через молоко, молочные продукты, кремы, овощные салаты). Бытовой путь реализуется, как правило, через бактерионосителей.
Патогенез и клинические особенности брюшного тифа и паратифов А и В .
1. Стадия внедрения возбудителя: сальмонеллы попадают в организм через рот и преодолев барьеры неспецифической защиты организма, проникают в тонкий кишечник, где происходит их адгезия к энтероцитам за счет пилей I типа.
2. Стадия поражения лимфоидной ткани: поражают пейеровы бляшки тонкого кишечника, в лимфатических фолликулах тонкой кишки сальмонеллы фагоцитируются макрофагами, с которыми проникают сначала в лимфоузлы, затем через грудной проток и в кровь.
3. Бактериемия (конец инкубационного периода): с током крови макрофаги вместе с поглощенными сальмонеллами циркулируют по организму (микроорганизмы могут даже в них размножаться).
4. Интоксикация: под воздействием бактерицидных факторов крови сальмонеллы погибают и при этом высвобождается эндотоксин, обусловливая лихорадку и сильнейшую интоксикацию, которая сохраняется на протяжение всего заболевания. (соответствует периоду выраженных клинических проявлений заболевания, температура тела достигает 39-400С и держится от 4 до 8 недель).
5. Стадия паренхиматозной диффузии: макрофаги с сальмонеллами циркулируют по организму и после гибели фагоцитов микробы могут попасть в различные органы: костный мозг, селезенку, печень, желчный пузырь, кожа и т.д. (воспаление, образование гранулем).
6. Выделительно-аллергическая стадия: вместе с желчью возбудители снова попадают в тонкий кишечник, при повторном контакте с сенсибилизированной лимфоидной тканью развивается гиперчувствительность немедленного типа (феномен Артюса), что приводит к некрозу пейеровых бляшек и образованию язв (кишечные кровотечения, прободение кишечника). По мере накопления антител организм постепенно освобождается от возбудителя – они выделяются со слюной, потом, испражнениями, желчью и мочой.
Инкубационный период – 10-14 дней. Клиника брюшного тифа, паратифов А и В характеризуется циклическим течением и проявляется лихорадкой (повышение температуры тела до 39-400С), интоксикацией, появлением розеолезной сыпи, гепатолиенальным синдромом,нарушениями со стороны нервной (бред, галлюцинации) и сердечно-сосудистой (падение АД, коллапс…) систем. Выздоровление не всегда совпадает с освобождением организма от возбудителей, этот процесс затягивается; 5 % переболевших становятся бактерионосителями.
Патогенез и клинические особенности сальмонеллезов .
Возбудители попадают в организм человека с обсемененными пищевыми продуктами. В желудке происходит частичная гибель сальмонелл. Воротами инфекции являются клетки слизистой тонкого кишечника. Здесь сальмонеллы внедряются между ворсинками, колонизируют и повреждают их. Это вызывает умеренное воспаление слизистой оболочки. Эндотоксин, выделяющийся при разрушении сальмонелл, обуславливает интоксикацию. Вырабатываемый сальмонеллами экзотоксин (энтеротоксин) вызывает диарею и рвоту, нарушение водно-солевого обмена и обезвоживание организма. Он обладает также цитотоксическим действием, вызывая гибель энтероцитов. Сальмонеллы проникают в подлежащие ткани слизистой оболочки, транспортируются через нее в макрофаги и могут поступать в лимфу и кровь, вызывая бактериемию и генерализацию инфекционного процесса.
Короткий инкубационный период – 12-24 часа. Начала заболевания – острое: озноб, повышение температуры до 390С, интоксикация (головная боль, слабость, тошнота), боли в животе, диспептические расстройства (рвота, понос), признаки обезвоживания организма, падение АД. Заболевание протекает обычно в течение 3-5 дней и заканчивается выздоровлением. При генерализованных формах сальмонеллез протекает более тяжело и длительно. Как субклиническую форму сальмонеллеза рассматривают бактерионосительство (острое – до 3 месяцев, хроническое – более 3 месяцев).
Постинфекционный иммунитет при брюшном тифе и паратифах – гуморальный, напряженный, длительный (не менее 15-20 лет, часто пожизненный). Образуются антитела к О-, Н-, Vi-антигенам:
* Первыми к концу 1-й недели заболевания появляются антитела к О-АГ, достигая максимума к периоду разгара (14-15 дней), а затем исчезают.
* Антитела к Н-АГ появляются к концу 2-й недели, достигая максимума в период реконвалесценции и длительно сохраняясь в организме после перенесенного заболевания.
* Антитела к Vi-АГ обнаруживаются у бактерионосителей брюшного тифа.
Постинфекционный иммунитет при сальмонеллезах – гуморальный и клеточный, типоспецифический, ненапряженный и недлительный, опосредован SIgA.
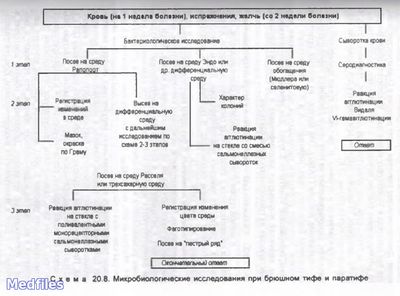
Микробиологические исследования при брюшном тифе и паратифе
Исследуемый материал: выбор материала для исследования при брюшном тифе и паратифах определяется стадией заболевания (инкубационный период – испражнения, продромальный период, 1-я неделя заболевания – кровь на посев, разгар заболевания и период реконвалесценции, с конца 2-ой недели – моча, испражнения, желчь, соскоб из розеол, костный мозг…, кровь на серодиагностику), при сальмонеллезах – испражнения, рвотные массы, промывные воды желудка, пищевые продукты, кровь.
1. Бактериоскопический метод.
2. Бактериологичекий метод (основной).
3. Серологический метод:
* Реакция Видаля (развернутая РА с О- и Н-антигенами);
* РНГА с эритроцитарными О-, Н-, Vi-диагностикумами;
4. Молекулярно-биологический метод (ПЦР, ДНК-зонды).
5. Аллергологический метод (кожно-аллергическая проба с эбертином).
Специфическая профилактика проводится по эпидпоказаниям:
— Вакцина ТАБТе – химическая сорбированная вакцина (содержит полные антигены брюшнотифозные, паратифозные А и В, столбнячный анатоксин);
— Брюшнотифозная спиртовая вакцина, обогащенная Vi- антигеном;
Неспецифическая профилактика : ранняя диагностика и изоляция больных, дезинфекция в очаге инфекции, выявление бактерионосителей, соблюдение санитарного режима в детских учреждениях, предприятиях питания, санитарно-бактериологический контроль за работой систем централизованного и нецентрализованного водоснабжения.
Лечение : ХТП и антибиотики; при сальмонеллезах применяется, в основном, патогенетическая терапия, направленная на нормализацию ВЭБ (антибиотики назначают только при генерализованных формах); спецефическое лечение – брюшнотифозные и сальмонеллезные бактериофаги.

.</p>
<p style=)