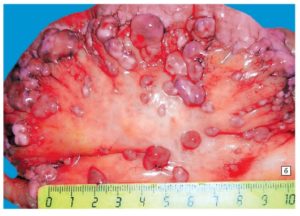
 Злокачественные новообразования любых органов могут привести к возникновению метастазов, а вторичные очаги существенно снижают шансы пациента на полное восстановление – к таким метастазам относится канцероматоз брюшины, основными проявлениями которого являются асцит, снижение веса и нарастающие симптомы интоксикации. Асцит – это гемморагический выпот, развивающийся с дессименацией по брюшине, которая возникает при злокачественных опухолях брюшной полости.
Злокачественные новообразования любых органов могут привести к возникновению метастазов, а вторичные очаги существенно снижают шансы пациента на полное восстановление – к таким метастазам относится канцероматоз брюшины, основными проявлениями которого являются асцит, снижение веса и нарастающие симптомы интоксикации. Асцит – это гемморагический выпот, развивающийся с дессименацией по брюшине, которая возникает при злокачественных опухолях брюшной полости.
Канцероматоз считается заболеванием с неблагоприятным прогнозом, при подобном осложнении, как правило, используется паллиативное (поддерживающее жизнедеятельность) лечение.
Канцероматоз брюшной полости. Что это такое?
Согласно МКБ-10 (Международной классификации болезней), канцероматоз – это вторичная, онкологическая патология, следствие распространения клеток рака из первичного очага.
Такой перенос обычно осуществляется с помощью лимфосистемы (лимфогенное заболевание), реже патология обуславливается прорастанием в брюшину первичной опухоли.
Раковые клетки, оказавшиеся в серозных полостях, закрепляются там и формируют образования, напоминающие по форме зерна проса. Эти новообразования постепенно расширяются, занимают новые площади, а результате сливаются, создавая внушительных размеров опухоль.
Ведущие клиники в Израиле



Этот злокачественный процесс нарушает экссудативную и резорбтивную функции серозной оболочки. Подобное изменение является причиной накапливания избыточной жидкости, что вызывает асцит.
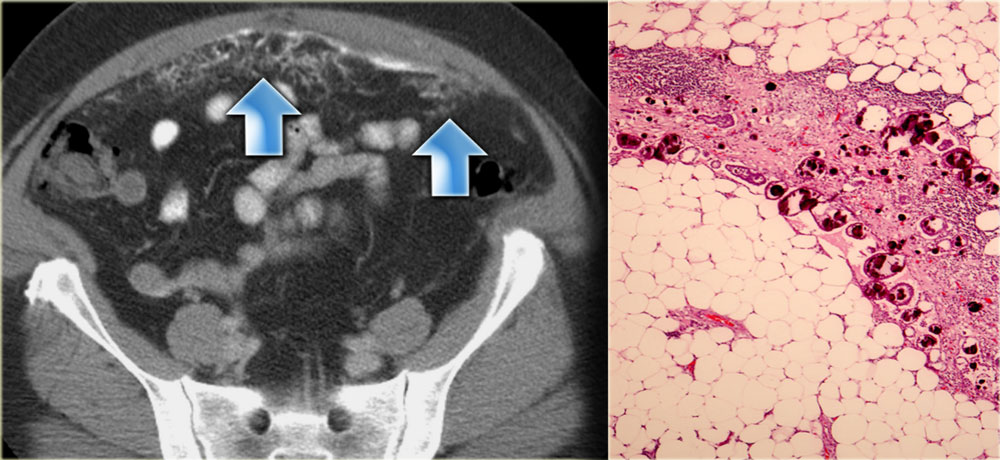 Обследование больных с канцероматозом брюшины выявило, что чаще всего данное осложнение встречается у пациентов с онкологией органов ЖКТ – поджелудочной железы, желудка.
Обследование больных с канцероматозом брюшины выявило, что чаще всего данное осложнение встречается у пациентов с онкологией органов ЖКТ – поджелудочной железы, желудка.
Второе место по распространенности причины возникновения патологии принадлежит раку яичников, и так как развитие карциноматоза брюшины возможно при раке яичников, это означает, что данному осложнению женщины подвержены гораздо чаще, чем мужчины.
Независимо от вида рака, поражение брюшины считается очень неблагоприятным признаком. И поскольку при подобном диагнозе невозможно использовать многие методики лечения, это может сказаться на вероятности успешного выздоровления пациента и сроке его жизни.
Также возможно образование карциноматоза плевральной полости. Оно характерно для рака легких, молочной железы, мезотелиомы плевры. Однако это состояние может обуславливаться любой опухолью, которая способна давать метастазы в плевру и легкие. Такие метастазы в плевре увеличивают проницаемость ее сосудов и нарушают отток лимфы, что может привести к накоплению жидкости и появлению канцероматозного плеврита.
Причины возникновения
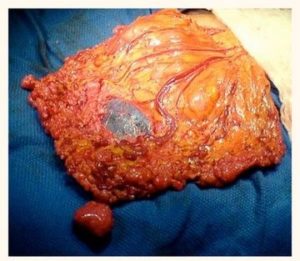 Главной причиной канцероматоза брюшины является уже имеющийся раковый очаг. В результате развития клетки опухоли неизбежно приобретают подвижность, вследствие чего они способны отделяться и перемещаться.
Главной причиной канцероматоза брюшины является уже имеющийся раковый очаг. В результате развития клетки опухоли неизбежно приобретают подвижность, вследствие чего они способны отделяться и перемещаться.
Распространение раковых клеток происходит:
- По кровотоку или с током лимфы;
- Через прорастание первичного новообразования в область брюшины;
- При оперативном хирургическом вмешательстве по удалению первичной опухоли.
Площадь серозной оболочки и всей брюшины может достигать 2 квадратных метров. Такие размеры определяют расположение непосредственно брюшины в брюшной полости, то есть у нее есть соприкасающиеся складки. Подобное строение способствует поражению значительной области брюшины при злокачественном процессе.
Ускоренному развитию канцероматоза брюшины способствуют следующие факторы:
- Постоянное соприкосновение складок брюшины;
- Соприкосновение брюшины с органами пищеварения;
- Наличие в органе обширной сети кровеносных и лимфатических сосудов.
Оказавшиеся в брюшине раковые клетки стремятся закрепиться в месте, где она меньше всего подвержена воздействию перистальтики кишечника. Также риск канцероматоза зависит от объемов первичной злокачественной опухоли и степени проникновения вглубь органа.
В случае недифференцированного рака желудка поражение брюшины опухолевыми клетками наблюдается у большей части пациентов.
Классификация и признаки канцероматоза
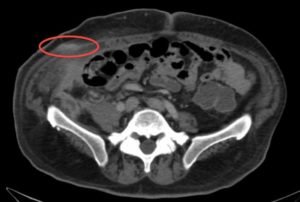 Поскольку канцероматоз брюшины – это вторичное поражение, сначала появляются симптомы, проявляющиеся при первичной опухоли. Однако иногда поставить диагноз рака позволяет именно клиническая картина поражения серозной оболочки.
Поскольку канцероматоз брюшины – это вторичное поражение, сначала появляются симптомы, проявляющиеся при первичной опухоли. Однако иногда поставить диагноз рака позволяет именно клиническая картина поражения серозной оболочки.
К основным симптомам, которые указывают на поражение брюшины, можно отнести:
1) Увеличение живота при резком снижении массы тела. Увеличение живота в размерах происходит из-за скопления жидкости – эта патология называется «асцит»;
2) Появление ноющих, тупых болей. Болевые ощущения могут быть постоянными или беспокоящими пациента периодами до нескольких дней;
3) Нарушения пищеварения. Проявляются тошнотой, коликами и болями в животе, также возможна рвота. Затрудняется опорожнение кишечника, иногда запор может сменяться поносом;
4) Симптомы интоксикации. Проливные поты, сильная слабость, повышение температуры, озноб, боли в голове и мышцах – этими симптомами характеризуется развивающийся канцероматоз.
Хотите получить смету на лечение?
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную смету на лечение.
У больного тяжелое общее состояние, такие пациенты нередко попадают в гастроэнтерологию или хирургию с диагностированным асцитом, причина которого выявляется позже.
Канцероматоз брюшины имеет классификацию, основанную на числе и локализации метастазов:
- Р1 – локальное поражение брюшины, ограниченное всего одним участком;
- Р2 – выявляется несколько очагов кацероматоза. Между данными очагами есть участки здоровой брюшины;
- Р3 – наблюдаются многочисленные, сливающиеся злокачественные очаги кацероматоза.
Видео — Карциноматоз брюшины: взгляд химиотерапевта
Диагностические мероприятия
В первую очередь онколог может заподозрить канцероматоз у людей, уже имеющих раковое заболевание в анамнезе.
Однако при снижении веса, болях в животе и прочих признаках онкологического образования врач должен в целях исключения либо подтверждения диагноза отправить пациента на диагностические процедуры.
Назначается:
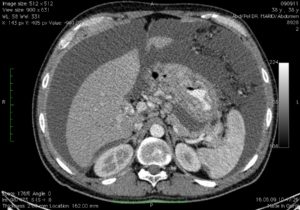
- Компьютерная томография. Послойное исследование брюшной области, выявление всех очагов патологии, их месторасположения, структуры;
- УЗИ брюшной полости и органов малого таза. Данный метод позволяет выявить первичную опухоль, их размеры и расположение, изменения в брюшине;
- МСКТ используется при оценке распространенности опухоли и для выявления поражений лимфоузлов;
- Анализ крови с высокой точностью устанавливает место расположения первичного очага;
- Лапароскопия позволяет как осмотреть брюшину, так и производить забор измененных тканей с целью проведения биопсии.
Примерно в 5-6% случаев при выявлении раковой опухоли возникают сложности, иногда она имеет настолько маленькие размеры, что не удается обнаружить ее прижизненно.
Как лечить канцероматоз брюшины?
 Лечение пациентов с канцероматозом достаточно сложное, а также оно не всегда оказывается достаточно эффективным. По возможности назначается операция в сочетании с химиотерапией.
Лечение пациентов с канцероматозом достаточно сложное, а также оно не всегда оказывается достаточно эффективным. По возможности назначается операция в сочетании с химиотерапией.
Также постоянно применяется и много других, инновационных методик лечения, так что нельзя с уверенностью сказать, что уже в ближайшем будущем не станет доступным эффективный способ лечения данной патологи. Тем не менее, народными средствами заболевание не вылечить.
Хирургическое лечение
Оперативное вмешательство (перитонэктомия) прежде всего заключается в удалении первичного ракового очага, пораженных лимфатических узлов, очагов осеменения раковыми клетками. Часто операция сочетается с удалением части тонкого или толстого кишечника, сигмовидной кишки, желчного пузыря, матки и придатков.
Химиотерапия при канцероматозе
При лечении больных с канцероматозом применяют одну из наиболее современных методик – гипертермическую интра перитонеальную химиотерапию.
Этот способ заключается во введении препаратов химиотерапии с помощью горячего воздуха прямо в брюшину, чего можно добиться в процессе операции.
Введенный раствор с химиотерапии препаратами продолжает находиться в брюшине примерно в течение часа, непрерывно циркулируя и уничтожая раковые клетки. Эффективность лечения увеличивается гипертермической химиотерапией в несколько раз.
Лечение первичного очага
 В случае канцероматоза брюшины следует выявить первичный очаг, а также оценить его локализацию, стадию и распространенность метастазов. Решение о необходимом лечении принимается только после проведения всех исследований.
В случае канцероматоза брюшины следует выявить первичный очаг, а также оценить его локализацию, стадию и распространенность метастазов. Решение о необходимом лечении принимается только после проведения всех исследований.
В случае, если стадия рака и локализация опухоли позволяют, проводится оперативное вмешательство по удалению образования (например, на 4 степени прогноз неблагоприятен). Дополнительно назначают сеансы лучевого облучения и химиотерапии.
Симптоматическая терапия
Это лечение, имеющее целью снижение или устранение основных симптомов заболевания. При канцероматозе, как правило, проводят:
- Обезболивание. В очень запущенных случаях боль моно снять только с помощью наркотического анальгетика;
- Лечение асцита. Оно заключается в удалении жидкости через имеющийся в брюшной стенке прокол;
- Улучшение функционирования органов пищеварения. Требуется улучшить усвояемость пищи и переваривание, усилить перистальтику;
- Вливание растворов. Внутривенное вливание имеет дезинтоксикационное действие, такое лечение нормализует состав крови;
- Применение мочегонных препаратов способствуют выводу лишней жидкости.
Если есть необходимость, то пациентам назначают препараты, улучшающие работу сердца и сосудов, спазмолитики, ферменты. Больной обязательно должен оставаться под наблюдением и периодически проходить повторный осмотр.
Сколько живут с диагнозом канцероматоз брюшины?
Обычно выявление заболевания происходит на последних стадиях. В таком случае при поражении брюшины продолжительность жизни больного составляет всего несколько лет, она зависит от тактики лечения первичного очага. Если была охвачена поражением большая часть брюшины, то справится с патологией невозможно и жить пациент будет всего несколько месяцев. Жизнеспособность поддерживается с помощью паллиативной методики, которая облегчает состояние человека.
Прогноз
Если заболевание было обнаружено в начале развития патологии, когда первичный очаг может быть удален, то прогноз благоприятный. Тогда необходимо придерживаться комплексной тактики лечения.
Если патология была выявлена на последних стадиях, то прогноз неблагоприятный, и независимо от лечения срок жизни существенно снижается. В таком случае проводится симптоматическое лечение, целью его действия является облегчение самочувствия пациента.
Канцероматоз брюшины – вторичное злокачественное поражение брюшины, являющееся следствием диссеминации эпителиальных опухолей желудочно-кишечного тракта, репродуктивной системы, реже – первичных перитонеальных новообразований. Признаками канцероматоза брюшины являются асцитический синдром, прогрессирующее снижение веса, тошнота, слабость. Диагностика основана на визуализации очагов поражения при проведении МСКТ, УЗИ органов брюшной полости, лапароскопии, цитологическом анализе асцитической жидкости. Лечение включает хирургическое удаление первичного очага с метастазами по брюшине и химиотерапию. Прогноз неблагоприятный.
Общие сведения
Канцероматоз брюшины – наиболее часто встречающийся вариант метастазирования онкологических заболеваний различной локализации. Согласно имплантационной теории развития данной патологии, источником поражения являются опухолевые клетки, которые отделились от первичного очага и попали в брюшную полость с серозной жидкостью. Основным пусковым механизмом данного процесса является утрата клетками опухоли факторов межклеточной адгезии.
Согласно данным статистики, канцероматоз брюшины встречается у 20-35% пациентов с онкопатологией: в 40% случаев данное осложнение формируется при опухолях желудочно-кишечного тракта, в 30% — при раке яичников (причем на момент верификации диагноза рака яичников у подавляющего большинства пациенток уже имеет место поражение брюшины). Канцероматоз брюшины является неблагоприятным прогностическим фактором; данная форма прогрессирующего опухолевого поражения практически не поддается хирургическому лечению, а химиотерапия улучшает состояние лишь на некоторое время.
Причины канцероматоза
Канцероматоз брюшины является вторичным опухолевым поражением, результатом прогрессирования рака различной локализации. Наиболее часто поражением брюшины осложняется рак желудка, тонкого кишечника, поджелудочной железы, злокачественные опухоли яичников, матки, маточных труб, печеночноклеточный рак, реже — первичные опухоли брюшины (перитонеальная мезотелиома). В ряде случаев первичный очаг остается неустановленным.
Развитие канцероматоза брюшины является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
- Р1 – локальное поражение брюшины
- Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
- Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы канцероматоза
Канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика
Канцероматоз брюшины имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики канцероматоза брюшины является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии канцероматоза брюшины без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение канцероматоза брюшины
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Системная химиотерапия при канцероматозе брюшины имеет определенные недостатки. На сегодняшний день эффективным методом лечения является интраперитонеальная химиотерапия. При местном введении цитостатических препаратов есть возможность применения высоких дозировок, которые при системной терапии слишком токсичны. Использование гипертермии усиливает поступление активных веществ в опухолевые клетки. Существенным преимуществом является длительное нахождение препарата в брюшной полости. Гипертермическая внутрибрюшная химиотерапия проводится в ходе операции или после ее завершения; химиотерапевтический агент (чаще препараты платины) вводится подогретым до температуры 40-43 градуса. Время циркуляции раствора составляет 30-90 минут.
Альтернативным методом лечения канцероматоза брюшины является фотодинамическая терапия с локальным или системным введением фотосенсибилизатора. Данная методика основана на интраоперационном световом воздействии с применением лазера, которое приводит к прямому повреждению мембран опухолевых клеток. Но такое лечение не устраняет процессы ангиогенеза, поэтому его эффективность недостаточно высока.
Ни один из существующих на сегодняшний день методов лечения канцероматоза брюшины не вызывает полную регрессию опухолевых диссеминантов, а также не предупреждает рецидивирование заболевания, поэтому разработка оптимального лечения продолжается. Исследуется таргетная терапия, целью которой являются молекулярные мишени. Низкая эффективность противоопухолевой терапии обусловлена отсутствием достаточного понимания морфологии и патогенеза заболевания, унифицированной классификации, разнородностью первичных опухолей.
Прогноз и профилактика
Развитие канцероматоза брюшины при злокачественных новообразованиях всегда является неблагоприятным прогностическим признаком. Средняя продолжительность жизни пациентов составляет не более 12 месяцев, а пятилетняя выживаемость – до 10%. Не существует специфической профилактики данной формы поражения брюшины, важную роль играет своевременность выявления и адекватного лечения первичных опухолей. Однако во многих случаях симптомы канцероматоза брюшины возникают уже при значительной диссеминации раковых клеток по брюшной полости.
Внутрибрюшная или интраперитонеальная гипертермическая химиотерапия и коротко HIPEC — современный метод лечения канцероматоза (опухолевого поражения) брюшины, который помогает существенно продлить жизнь пациента. HIPEC представляет собой комбинацию двух методов противоопухолевого лечения: гипертермии — повышения температуры тела одновременно с химиотерапией, а фактически длительное промывание подогретым до 42-43°С раствором цитостатика внутренних органов и покрывающих их листков брюшины.
Что собой представляет брюшина
Брюшина — тонкая «обертка» из соединительной ткани, которая выстилает стенки брюшной полости и покрывает внутренние органы. Состояние, при котором на поверхности брюшины растпространяются раковые клетки, называется канцероматозом. Если у пациента диагностирована такая патология, его прогноз сильно ухудшается.
Чаще всего поражение брюшины происходит метастазами из других органов, например, толстой кишки, желудка, яичника. Реже встречаются первичные опухоли брюшины — мезотелиомы, псевдомиксомы.
В зависимости от происхождения опухолевых очагов, средняя продолжительность жизни при канцероматозе брюшины и отсутствии лечения составлет от 6 недель до 6 месяцев.

Когда может быть полезна интраперитонеальная гипертермическая химиотерапия?
Методика HIPEC применяется при метастатическом поражении слизистой оболочки, покрывающей полость живота — канцероматозе брюшины.
Доступные ранее методы лечения были несовершенны. Во время циторедуктивной операции хирург может удалить только видимые опухолевые очаги, но микроскопические остаются, и это приводит к рецидиву. Если вводить химиопрепараты после операции внутривенно, то они плохо достигают опухолевых клеток в брюшине. Нужны очень большие дозы, они вызывают тяжелые побочные эффекты.
С 90-х годов прошлого века начал развиваться новый метод лечения — HIPEC (Hyperthermic Intraperitoneal Chemotherapy), гипертермическая интраперитонеальная химиотерапия. Брюшную полость промывают подогретым раствором химиопрепаратов прямо на операционном столе, после циторедуктивного вмешательства. За счет этого удалось существенно повысить эффективность лечения и выживаемость пациентов.
В чем преимущества HIPEC?
- За счет локального воздействия можно применять более высокие дозы противоопухолевых препаратов. В системный кровоток попадает лишь небольшое количество лекарства, за счет этого снижается риск побочных эффектов.
- Высокая температура сама по себе уничтожает опухолевые клетки за счет денатурации (изменения трехмерной структуры) белков и других молекул, нарушения синтеза и репарации ДНК, важных биохимических процессов в клетках.
- За счет нагревания улучшается проникновение препарата в опухолевые очаги.
- Раствор в брюшной полости вымывает свободные опухолевые клетки и сгустки крови, на которых они могут быть зафиксированы.
- Внутри опухолевых очагов клетки могут находиться в состоянии гипоксии – кислородного голодания. Они нечувствительны к лучевой терапии, но чувствительны к нагреванию.
- Высокая температура заставляет опухолевые клетки активно размножаться, за счет этого на них лучше действуют химиопрепараты.
- Есть некоторые данные о том, что нагревание подавляет рост новых кровеносных сосудов в опухолевых очагах и стимулирует противоопухолевый иммунитет за счет выработки белков теплового шока.
До появления HIPEC средняя выживаемость пациентов с мезотелиомой брюшины составляла 6 месяцев. В 2018 году были опубликованы результаты исследования в научном журнале International Journal of Hyperthermia. Авторы работы оценили применение гипертермической интраперитонеальной химиотерапии у 76 пациентов с мезотелиомой. Медиана безрецидивной выживаемости составила почти 5 лет, а медиана общей выживаемости – более 8 лет.

При каких заболеваниях помогает HIPEC?
На данный момент имеются доказательства эффективности гипертермической интраперитонеальной химиотерапии при первичных опухолях брюшины и ее поражении метастазами при раке, возникающем в различных органах.
Первичные опухоли брюшины:
Метастазы из других органов:
- Колоректальный рак (толстой и прямой кишки);
- Рак яичников;
- Опухоли аппендикса (червеобразного отростка);
- Рак печени;
- Рак поджелудочной железы.
Как проводится процедура?
В разных клиниках технология проведения HIPEC может различаться. Применяют разные химиопрепараты и их сочетания, разные температуры, объемы раствора для промывания брюшной полости. Но общие моменты везде одинаковы, лечение состоит из двух этапов.
Этап I. Циторедуктивная операция
HIPEC – дополнение к хирургическому вмешательству, она не может быть эффективна без предшествующей операции. Сначала хирург должен удалить все крупные, видимые опухолевые очаги. Для этого полностью или частично удаляют все пораженные органы, участки брюшины, выстилающей стенки брюшной полости. Затем органы, на которых было проведено вмешательство, восстанавливают, например, накладывают анастомозы – сшивают концы кишки, если был удален ее участок.
Это довольно сложное хирургическое вмешательство. Хирург должен обладать достаточным опытом и профессионализмом, чтобы правильно оценить ситуацию, обеспечить максимальную циторедукцию (удалить все очаги). А пациент должен иметь достаточно хорошее здоровье, чтобы перенести операцию.
Этап II. Гипертермическая интраперитонеальная химиотерапия
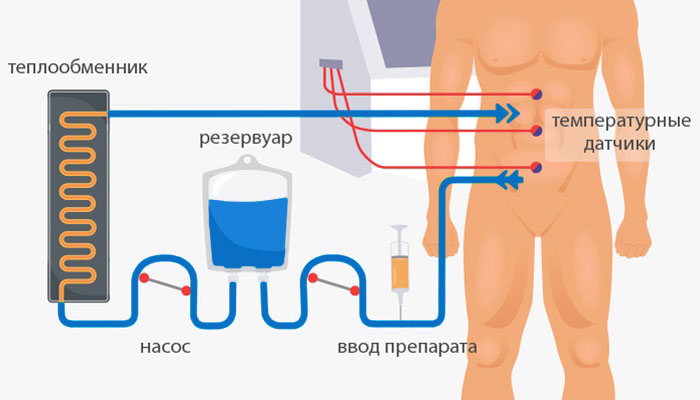
После того как операция завершена, в определенных местах в брюшной полости устанавливают катетеры и подсоединяют их к перфузионной системе, которая обеспечивает подачу нагретого раствора химиопрепарата. Кроме того, в брюшную полость пациента помещают датчики для контроля температуры.
Для того чтобы HIPEC принесла нужный эффект, брюшную полость нужно промывать в течение 1–1,5 часа. Вместе с хирургическим вмешательством лечение может продолжаться от 6 до 18 часов.
По прошествии необходимого времени из брюшной полости удаляют раствор лекарства и промывают её физраствором. Катетеры и температурные датчики вынимают, накладывают швы.
Для всех ли пациентов с канцероматозом брюшины подходит HIPEC?
Гипертермическая интраперитонеальная химиотерапия – процедура, которая подходит не для всех пациентов, и не все могут ее перенести. Для проведения этого вида лечения нужно, чтобы соблюдались некоторые условия:
- Возраст и сопутствующие заболевания пациента не должны создавать высоких рисков во время хирургического вмешательства. Больной должен пройти тщательное и всестороннее предоперационное обследование.
- Все опухолевые очаги должны быть резектабельными, то есть их в принципе можно удалить.
- Распространение рака должно быть ограничено только брюшной полостью. Если есть отдаленные метастазы в других органах, например, в головном мозге, костях, то лечение будет неэффективным.
- Вся брюшина не должна быть покрыта очагами, имеющими размеры более 2,5 см.
Показания и противопоказания для HIPEC определяются в каждом случае индивидуально. Если вы хотите узнать, подходит ли этот метод лечения в вашем случае – запишитесь на консультацию к врачу в клинике Медицина 24/7.
Для того чтобы понять, насколько эффективным будет лечение, врачи определяют индекс опухолевого поражения брюшины (peritoneal cancer index, PCI). Для этого брюшную полость делят на 13 областей и оценивают размеры опухолевых узлов в них по трехбалльной шкале:
- 0 баллов – очаги не обнаружены;
- 1 балл – очаги до 0,5 см;
- 2 балла – очаги до 5 см;
- 3 балла – очаги более 5 см.
Деление брюшной полости на области выглядит следующим образом:
Что происходит после HIPEC?
Результаты лечения различаются в зависимости от типа злокачественной опухоли, количества и размеров очагов в брюшной полости, других факторов. Например, при псевдомиксоме прогноз лучше, чем при колоректальном раке и злокачественной мезотелиоме.
Потенциально HIPEC может уничтожить все опухолевые клетки и полностью вылечить пациента. Тем не менее, даже если излечения достичь не удается, существенно увеличивается продолжительность жизни: она составляет годы вместо месяцев.
Раньше, для того чтобы пройти HIPEC, пациенты из России были вынуждены ехать в зарубежные клиники. Сейчас эта методика доступна и в Москве. В клинике Медицина 24/7 процедуру проводят опытные хирурги-онкологи и химиотерапевты, проходившие обучение в ведущих онкологических центрах за границей. Свяжитесь с нами и получите консультацию нашего врача-специалиста.
Какие осложнения возникают после HIPEC?
Любое оперативное вмешательство на органах брюшной полости может осложниться кровотечением, инфекцией послеоперационной раны, реактивным воспалением внутренних органов. Осложнения обусловлены объёмом хирургического вмешательства, исходным состоянием пациента, локализацией метастатических очагов и биохимическими изменениями, возникающими из-за присутствия в организме злокачественного процесса.
Понятно, что ни химиотерапия, ни гипертермия не улучшают процесс послеоперационного восстановления и не помогают поддержанию иммунитета, тем не менее, частота смертельных осложнений невысока — не превышает 3%. Обусловленные токсическими эффектами химиотерапии реакции, как правило, выражены меньше, чем при внутривенном введении.
Хороший результат не случайность, а система только в руках опытного специалиста, сделавшего сотни стандартных операций и умеющего нестандартно мыслить, обеспеченного классным оборудованием и оригинальными лекарствами. Хорошему хирургу-онкологу необходима команда коллег-единомышленников, помогающих в работе ему и в восстановлении — пациентам. Всё это есть в клинике Медицина 24/7 в Москве.
Войцеховский Валерий Владимирович, Гоборов Николай Дмитриевич, Григоренко Алексей Александрович, Ландышев Юрий Сергеевич, Лазуткина Елена Леонидовна Особенности диагностики злокачественной мезотелиомы плевры // Бюл. физ. и пат. дых.. 2016. №60.
Хирургические болезни: учебник / под редакцией А. Ф. Черноусова. М.: ГЭОТАР-МЕДИА, 2010. — 664 с.: ил. + CD — ISBN 978-5-9704-1278-7

