Механизм всасывания аминокислот и низкомолекулярных пептидов – сложный биологический процесс, который включает взаимодействие аминокислот и пептидов с мембранами клеток, формирующих ворсинки слизистой оболочки, их транслокацию через мембраны и высвобождение в кровь. Считается, что этот процесс обеспечивается специфическими переносчиками. Трансмембранная транслокация аминокислот происходит преимущественно против градиента их концентрации и является энергозависимым процессом. В процессе всасывания важная роль принадлежит натриевому насосу.
Одним из механизмов транспорта аминокислот является -глутамильный цикл. Ключевой фермент процесса — -глутамилтрансфераза. Этот фермент катализирует перенос глутамильного остатка глутатиона на транспортируемую кислоту:
аминокислота + глутатион (глутамилцистеинилглицин) глутамиламинокислота + цистеинилглицин
Свободная аминокислота, участвующая в этой реакции, поступает с наружной поверхности клетки, глутатион находится внутри. После реакции глутамиламинокислота оказывается в клетке вместе с цистеинилглицином. Далее эта кислота расщепляется ферментом цитозоля глутамиламинотрансферазой: глутамиламинокислота аминокислота + 5-оксопролин.
В итоге молекула аминокислоты оказывается в цитозоле.
Благодаря высокой проницаемости слизистой кишечника новорожденных и низкой концентрации у них протеолитических ферментов может всасываться некоторое количество нативных белков, обуславливающих сенсибилизацию организма.
Всасываемые в тонком отделе кишечника аминокислоты попадают в портальный кровоток и, следовательно, в печень, а затем в общий кровоток. Кровь освобождается от аминокислот очень быстро – уже через 5 минут 85 – 100 % их оказывается в тканях. Особенно интенсивно поглощают аминокислоты печень и почки.
Пути использования аминокислот в организме животных
Использование аминокислот в организме животных осуществляется по следующим направлениям (рис. 16):
для синтеза белков и пептидов;
для образования других аминокислот и азотсодержащих соединений;
для синтеза углеводов (глюкогенные аминокислоты) и липидов (кетогенные аминокислоты);
как источник энергии.
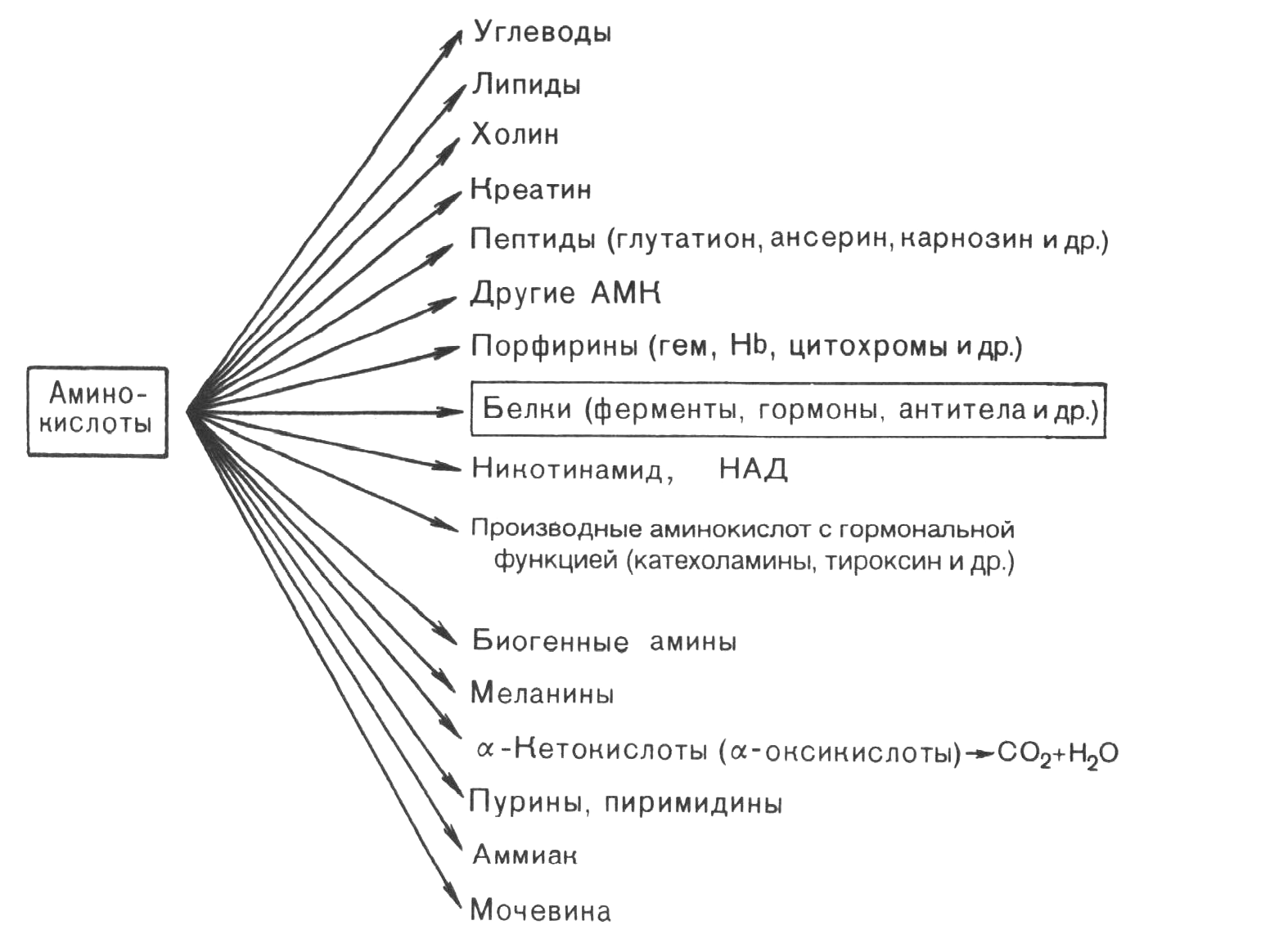
Рис. 16. Пути использования аминокислот в тканях организма животных.
Во 2-м и 3-м случаях аминокислоты теряют аминогруппу, а их безазотистый углеродный скелет превращается в один из следующих промежуточных продуктов метаболизма – пируват, оксалоацетат, -кетоглутарат, сукцинил-КоА, фумарат, ацетил-КоА, ацетоацетил-КоА (для каждой аминокислоты свой промежуточный продукт).
Те аминокислоты, безазотистые остатки которых превращаются в один из первых пяти веществ называются глюкогенными, потому что эти соединения через фосфоенолпируват далее вовлекаются в глюконеогенез (рис. 17). К глюкогенным аминокислотам относятся глицин, серин, -аланин, цистеин, валин, метионин, треонин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, аргинин, пролин, гистидин.
К кетогенным относятся аминокислоты, безазотистые углеродные остатки которых превращаются в ацетил-КоА или ацетоацетил-КоА, которые далее включаются в кетогенез.
Кетогенной аминокислотой является лейцин.
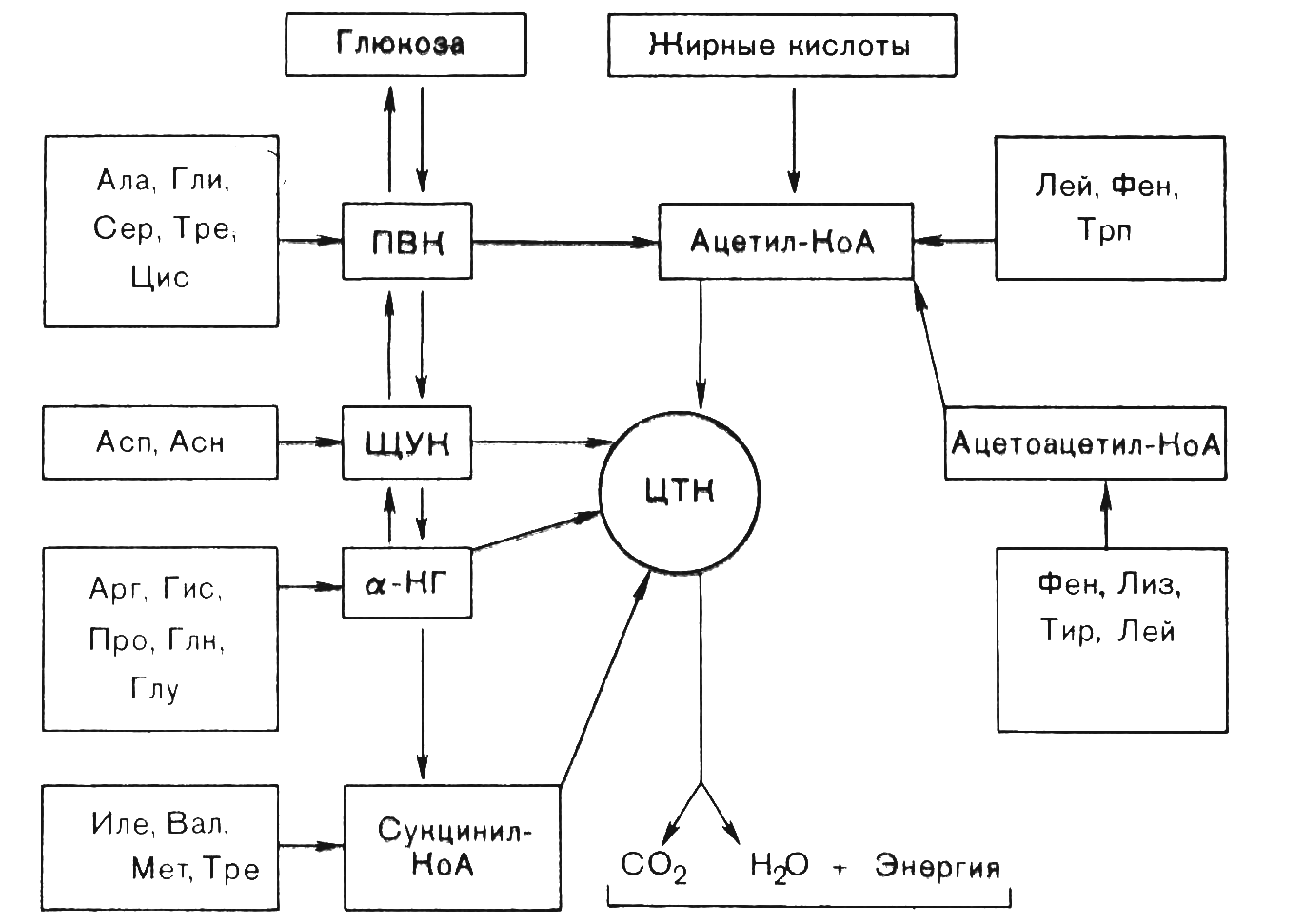
Рис. 17. Сема включения аминокислот в ЦТК и в глюконеогенез.
Изолейцин, лизин, триптофан, фенилаланин и тирозин относятся одновременно и к кетогенным и к глюкогенным аминокислотам. Некоторые из их углеродных атомов обнаруживаются в ацетил-КоА или ацетоацетил-КоА, тогда как другие появляются в потенциальных предшественниках глюкозы.
Избыток аминокислот относительно того их количества, которое требуется для синтеза белков и других биомолекул, в отличие от глюкозы и жирных кислот не может запасаться и не выделяется из организма. Избыточные аминокислоты используются как метаболическое топливо (конечные продукты распада аминокислот – NH3, выделяющийся из организма в виде мочевины, СО2, Н2О и АТФ).
Всасывание аминокислот в кишечнике — раздел Химия, Курс лекций по общей биохимии ВсаСывание L-Аминокислот (Но Не D) — Активный Процесс, В Результате Которого.
Всасывание L-аминокислот (но не D) — активный процесс, в результате которого аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Известно пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
1. нейтральных, короткой боковой цепью (аланин, серии, треонин);
2. нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолейцин);
3. с катионными радикалами (лизин, аргинин);
4. с анионными радикалами (глутаминовая и аспарагиновая кислоты);
5. иминокислот (пролин, оксипролин).
Существуют 2 основных механизма переноса аминокислот: симпорт с натрием и γ-глутамильный цикл.
1. Симпорт аминокислот с Na + .
Симпортом с Nа + переносятся аминокислоты из первой и пятой группы, а также метионин.
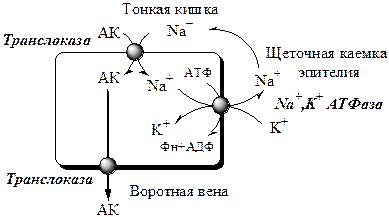
L-аминокислота поступает в энтероцит путём симпорта с ионом Na +. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично-активного транспорта с помощью Na + , К + -АТФ-азы.
Эта тема принадлежит разделу:
Курс лекций по общей биохимии
Гоувпо угма федерального агентства по здравоохранению и социальному развитию.. кафедра биохимии..
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Всасывание аминокислот в кишечнике
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
Все темы данного раздела:
Роль белка в питании. Показатели качества пищевого белка
Роль белка в питании: основной источникАК, в первую очередь незаменимых. Богаты белками продукты животного происхождения: мясо, рыба, сыр. Продукты растительного происхождения соде
Азотистый баланс. Принципы нормирования белка в питании. Белковая недостаточность
Азотистый баланс– разница между количеством азота, поступающего с пищей, и количеством выделяемого азота. Азот преимущественно поступает в организм в виде АК (95%), а выделяетс
Нормы белка в питании
· Для здорового взрослого человека минимальное количество белка в пище составляет 30-50 г/сут (при биологической ценности не ниже 70%). Оно поддерживает азотистое равновесие, но не обеспечивает сох
Белковая недостаточность
Продолжительное безбелковое питание вызывает серьёзные нарушения обмена веществ и неизбежно заканчивается гибелью организма. Дефицит в пище даже одной незаменимой АК ведёт к неполному усвоению др
Переваривание белков в ЖКТ
Переваривание – процесс гидролиза веществ до их ассимилируемых форм. Всасывание – процесс поступления веществ из просвета ЖКТ в кровеносное русло.
Переваривание белков в желудке
Желудок выполняет несколько функций: защитную (обезвреживание пищи: HCl, лизоцим), переваривание (механическая и химическая обработка пищи: HCl, ферменты), всасывание, эндокринную (образование гаст
Состав желудочного сока
Неорганические вещества Кол-во Органические вещества Кол-во Свободная НС1 20 ммоль/л, 0,4-0,5%
Механизм образования соляной кислоты
Согласно карбоангидразной теории, источником Н+ для HCl является Н2СО3, которая образуется в обкладочных клетках желудка из СО2 и Н2О под дей
Ферменты желудка
Пепсиноген неактивный фермент, синтезируется в главных клетках, состоит из одной полипептидной цепи с молекулярной массой 40 кД. В просвете желудка под действием НС1
Определение кислотности желудочного сока
Кислотность желудочного сока выражается в титрационных единицах (Т.Е.), определяется количеством мл 0,1Н раствора NaOH, пошедшего на титрование 100 мл желудочного сока. Титрование проводят в присут
Переваривание белков в кишечнике
Функции тонкой и толстой кишок: 1). завершение переваривания всех компонентов пищи; 2). всасывание образовавшихся соединений; 3). удаление непереваренных продуктов (формирование каловых масс и их э
Панкреатический сок
Для пищеварения в поджелудочной железе синтезируется сложный по составу сок, который представляет собой бесцветную опалесцирующую жидкость с величиной рН=7,5-8,8. В сутки выделяется 1,5-2,5 литра с
Специфичность действия протеаз
Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее активны в отно
Кишечный сок
Кишечный сок является продуктом деятельности всей слизистой оболочки кишечника и представляет собой неоднородную вязкую жидкость, с величиной рН=7,2-8,6 (с усилением секреции рН повышается). За сут
Защита клеток от действия протеаз
Клетки поджелудочной железы защищены от действия пищеварительных ферментов тем, что: · эти ферменты образуются в клетках поджелудочной железы в неактивной формеи активируются только после
Регуляция желудочно-кишечной секреции
Натощак секретируется незначительное количество желудочного сока. Регуляция секреции желудочного сока осуществляется в 3 фазы: 1. Мозговая (сложнорефлекторная)
Регуляция поджелудочной секреции
Регуляция секреции поджелудочного сока осуществляется в 3 фазы: 1. Мозговая (сложнорефлекторная) фаза. Осуществляется через комплекс условных и безусловных рефлексов. Вид, запах и в
Регуляция кишечной секреции
Регуляция деятельности желез тонкой кишки осуществляется местными нервно-рефлекторными механизмами, а также гуморальными влияниями и ингредиентами химуса. Механическое раздражение слизистой оболочк
Глутамильный цикл
γ-глутамильный цикл переносит некоторые нейтральные аминокислоты (фенилаланин, лейцин) и аминокислоты с катионными радикалами (лизин) в кишечнике, почках и, по-видимому, мозге. В эт
Нарушение переваривания белков и транспорта аминокислот
Непереносимость белков пищи (например, молока и яиц) у взрослых людей. В норме у взрослых людей из кишечника кровь попадают только лишенные антигенных свойств аминокислоты.
Гниение
Гниение– (putrefacio) процесс расщепления азотсодержащих, главным образом белковых веществ, в результате жизнедеятельности микроорганизмов. В аэробных условиях белковые мо
ЛЕКЦИЯ № 18
Тема: Белки II. Общие пути обмена аминокислот. Биосинтез мочевины. Факультеты: лечебно-профилактический, медико-профилактический, педиатрический. 2 курс.
Физико-химические свойства аминокислот
АК белые кристаллические вещества, хорошо растворимые в воде. Имеют высокую температуру плавления, в твердом состоянии находятся в виде внутренней соли. Многие сладкие на вкус (гли). АК ам
И его использование в организме
Большая часть аминокислот организма человека, примерно 15кг, входит в состав белков. Фонд свободных АК организма составляет примерно 35г. Источниками АК в организме являются белки пищи, бе
Трансаминирование (переаминирование) аминокислот
Трансаминирование — реакция переноса α-аминогруппы с АК на α-кетокислоту, в результате чего образуются новая α-кетокислота и новая АК. Процесс трансаминирования легко обратим, при не
Механизм переаминирования
Вначале, АК передает свою аминогруппу на пиродоксальфосфат. АК при этом превращ
Органоспецифичные аминотрансферазы АЛТ и АСТ
Чаще всего в трансаминировании участвуют АК и кетокислоты, которых много в организме — глу, ала, асп, α-КГ, ПВК и ЩУК. Основным донором аминогруппы служит глу, а кетогруппы — α-КГ.
Прямое дезаминирование АК
Прямое дезаминирование — это дезаминирование, которое происходит в 1 стадию с участием одного фермента. Прямому дезаминированию повергаются глу, гис, сер, тре, цис.
Внутримолекулярное дезаминирование
Внутримолекулярное дезаминирование характерно для гистидина. Реакцию катализирует гистидаза (гистидин-аммиаклиаза). Эта реакция происходит только в печени и коже.
Непрямое дезаминирование в печени
Непрямое дезаминирование АК происходит при участии 2 ферментов: аминотрансферазы и глу-ДГ. Аминогруппы АК в результате трансаминирования переносятся на α-КГ с образованием глутамата, который з
Непрямое дезаминирование в мышцах (и нервной ткани)
В мышечной ткани активность глу-ДГ низка, поэтому при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ.
Пути обмена безазотистого остатка аминокислот
За сутки у человека распадаются примерно 100г АК. Катаболизм всех АК сводится к образованию шести веществ, вступающих в общий путь катаболизма: ПВК, ацетил-КоА, α-кетоглутарат, сукцинил-КоА, ф
Токсичность аммиака
Аммиак — токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное действие на организм, и, прежде всего на ЦНС. Механизм токсического действия амми
Обмен глутамата
В мозге и некоторых других органах может протекать восстановительное аминирование α-кетоглутарата под действием глутаматдегидрогеназы, катализирующей обратимую реакцию.
Обмен глутамина
Основной реакцией связывания аммиака, протекающей во всех тканях организма (основные поставщики мышцы, мозг и печень), является синтез глутамина под действием глутаминсинтетазы:
Обмен аланина
Из мышц и кишечника избыток аминого азота выводится преимущественно в виде аланина. В кишечнике:
Орнитиновый цикл
Большая часть свободного аммиака, а также аминного азота в составе АК (в основном глутамин, аланин) поступают в печень, где из них синтезируется нетоксичное и хорошо растворимое в воде соединение —
Реакции орнитинового цикла
Предварительно в митохондриях под действием карбамоилфосфатсинтетазы I с затратой 2 АТФ аммиак связывается с СО2 с образованием карбамоилфосфата:
Регенерация аспартата из фумарата
Фумарат, образующийся в орнитиновом цикле, в цитозоле превращается в ЩУК, который переаминируется с аланином или глутаматом с образованием аспартата. Аланин поступает главным образом из мышц и клет
Энергетический баланс орнитинового цикла
На синтез 1 мочевины расходуются 4 макроэргических связи 3 АТФ. Дополнительные затраты энергии связаны с трансмембранным переносом веществ и экскрецией мочевины. Энергозатраты при этом частично ком
Гипераммониемия
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови — гипераммониемию, что оказывает токсическое действие на организм. Причи
Наследственные нарушения орнитинового цикла и их основные проявления
Заболевание Дефект фермента Тип наследования Клинические проявления Метаболиты кровь
Декарбоксилирование аминокислот и их производных
Некоторые АК и их производные могут подвергаться декарбоксилированию – отщеплению α-карбоксильной группы. У млекопитающих декарбоксилируются: три, тир, вал, гис, глу, цис, арг, орнитин, SAM, Д
Гистамин
Гистамин образуется в тучных клетках. Секретируется в кровь при повреждении ткани, развитии иммунных и аллергических реакций.
Фолиевая кислота
Значительную роль в обмене ряда АК, синтезе некоторых сложных липидов, нейромедиаторов, гормонов и ряда других веществ играют производные фолиевой кислоты. Фолиевая кислота
Образование одноуглеродных фрагментов, их взаимопревращения
ТГФК принимает от АК одноуглеродные фрагменты: серин и глицин дают метиленовый фрагмент (-СН2-), гистидин – формимино- и формильный фрагменты. В составе ТГФК одноуглеродные фраг
Недостаточность фолиевой кислоты
Гиповитаминоз фолиевой кислоты возникает редко, его вызывает использование сульфаниламидных препаратов. Сульфаниламиды — структурные аналоги парааминобензойной кислоты, они ингибируют синтез фолие
Обмен серина и глицина
Серин и глицин — заменимые аминокислоты. Синтез серина:
Наследственные нарушения обмена глицина
Известно несколько заболеваний, связанных с нарушениями обмена глицина. В их основе лежит недостаточность ферментов или дефект системы транспорта этой АК. Гиперглицинемия
Цистеин
Цистеин – серосодержащая условнозаменимая АК. Синтезируется из незаменимого метионина и заменимого серина. Нарушение синтеза цистеина возникает при гиповитаминозе фоли
Фенилаланин
Фенилаланин — незаменимая АК, которая содержится в достаточных количествах в пищевых продуктах. Фенилаланин идет в основном на синтез белков и тирозина.
Фенилкетонурия
В печени здоровых людей небольшая часть фенилаланина (10%) превращается в фениллактат и фенилацетилглутамин. При дефекте фенилаланингидроксилазы этот путь катаболизма фенила
Обмен тирозина в надпочечниках и нервной ткани
В мозговом веществе надпочечников и нервной ткани тирозин метаболизирует по катехоламиновому пути с образованием дофамина, норадреналина и адреналина (только в надпочечниках
Болезнь Паркинсона
Болезнь Паркинсона развивается при снижении активности тирозинмонооксигеназы и ДОФА-декарбоксилазы, что приводит к недостаточности дофамина в чёрной субстанции мозга. Это одно
Обмен тирозина в меланоцитах
В пигментных клетках (меланоцитах) обмен тирозин идет по меланиновому пути. Из тирозина синтезируются пигменты — меланины 2 типов: эумеланины и феомеланины. Эумел
Катаболизм тирозина в печени
Катаболизм тирозина происходит в печени по гомогентизиновому пути (схема).
Тирозинемии
Некоторые нарушения катаболизма тирозина в печени приводят к тирозинемии и тирозинурии. Различают 3 типа тирозинемии. 1.Тирозинемия типа 1 (тирозиноз). Причиной заболе
Использование глутамата
1. Используется в синтезе белков, липидов, углеводов; 2. Ведущая роль в интеграции азотистого обмена. Обеспечивает реакции переаминирования АК: глутамат универсальный донор аминогруппы для
Всасывание аминокислот в кишечнике
Всасывание L-аминокислот (но не D-) — это активный процесс, в результате которого аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Известно пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
1) нейтральных, короткой боковой цепью (аланин, серии, треонин);
2) нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолейцин);
3) с катионными радикалами (лизин, аргинин);
4) с анионными радикалами (глутаминовая и аспарагиновая кислоты);
5) иминокислот (пролин, оксипролин).
Механизм переноса аминокислот в эпителиальные клетки кишечника
Существуют 2 основных механизма переноса аминокислот: 1) симпорт с натрием и 2) γ-глутамильный цикл.
1. Симпорт аминокислот с Na+.
Симпортом с Nа+ переносятся аминокислоты из первой и пятой группы, а также метионин.

L-аминокислота поступает в энтероцит путём симпорта с ионом Na+. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично-активного транспорта с помощью Na+,К+-АТФ-азы. Таким образом, для такого переноса аминокислот используется энергия электрохимического потенциала ионов натрия, запасённая им в процессе выдворения его из клетки натрий-калиевым насосом (Na+,К+-АТФ-азой) против градиента концентрации. Энтероциты в этом используют тот же механизм, что и нейроны при формировании потенциала покоя.
2. γ-Глутамильный цикл.
Более изощрённый по сравнению с симпортом γ-глутамильный цикл переносит некоторые нейтральные аминокислоты (фенилаланин, лейцин) и аминокислоты с катионными радикалами (лизин) в кишечнике, почках и, по-видимому, мозге.

В этой системе участвуют 6 ферментов, один из которых находится в клеточной мембране, а остальные — в цитозоле. Мембранно-связанный фермент γ-глутамилтрансфераза (гликопротеин) катализирует перенос γ-глутамильной группы от глутатиона на транспортируемую аминокислоту и последующий перенос комплекса в клетку. Аминокислота отщепляется от у-глутамильного остатка под действием фермента у-глутамилциклотрансферазы.
Дипептид цистеинилглицин расщепляется под действием пептидазы на 2 аминокислоты — цистеин и глицин. В результате этих 3-х реакций происходит перенос одной молекулы аминокислоты в клетку (или внутриклеточную структуру). Следующие 3 реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно. Для транспорта в клетку одной молекулы аминокислоты с участием у-глутамильного цикла затрачиваются 3 молекулы АТФ. Важно отметить эти заметные потери энергии, затраченной на всасывание аминокислот при белковом питании.
Поступление аминокислот в организм осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Максимальная концентрация аминокислот в крови достигается через 30—50 мин после приёма белковой пищи (углеводы и жиры замедляют всасывание аминокислот). Аминокислоты при всасывании конкурируют друг с другом за специфические участки связывания. Например, всасывание лейцина (если концентрация его достаточно высока) уменьшает всасывание изолейцина и валина.
